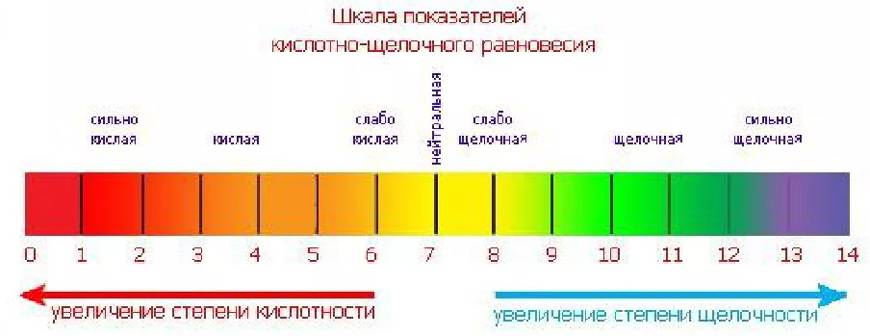
Почему растет pH в бассейне
Если показатель рН выше отметки 7,5 единиц, то можно говорить о высокой щелочности воды. Она повышается по нескольким причинам:
- при строительстве спортивных бассейнов установили фильтр для повышения рН, он рассчитан на применение в кислых средах, а используется для жидкости с нормальными показателями;
- из-за большого количества купающихся;
- неправильно применяются средства для нормализации кислотно-щелочного баланса.
Повышенный рН приводит к:
- кальциевым отложениям на оборудовании и трубах;
- ускорению биологических процессов и роста микроорганизмов;
- ухудшению состояния кожи и слизистых пловцов;
- снижению результативности химии для бассейна, что влечет увеличенный расход препаратов и дополнительные расходы.
Жидкость с высоким содержанием щелочи становится мутной, «мыльной», хлорсодержащие средства и активный кислород выпадают в осадок в виде хлопьев.
Измерение pH
Для определения pH растворов применяют специальные реактивы – индикаторы, а также приборы – pH-метры (электрометрическое определение pH).
Индикаторное определение pH. Чаще всего в аналитической практике pH растворов определяют приближенно с помощью реактивной индикаторной бумаги (в интервале 0,5-2,0 единицы pH). С помощью индикаторной универсальной бумаги можно определить pH более точно (в интервале 0,2-0,3 единицы pH). В табл. 7 и 8 приведены данные о реактивных и универсальных индикаторных бумагах.
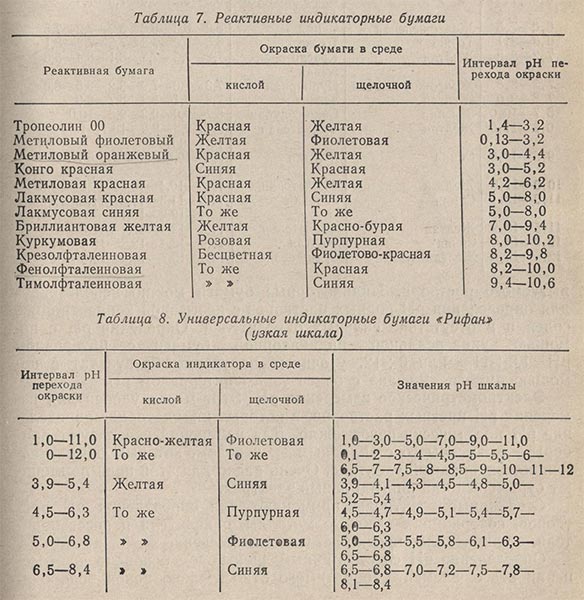
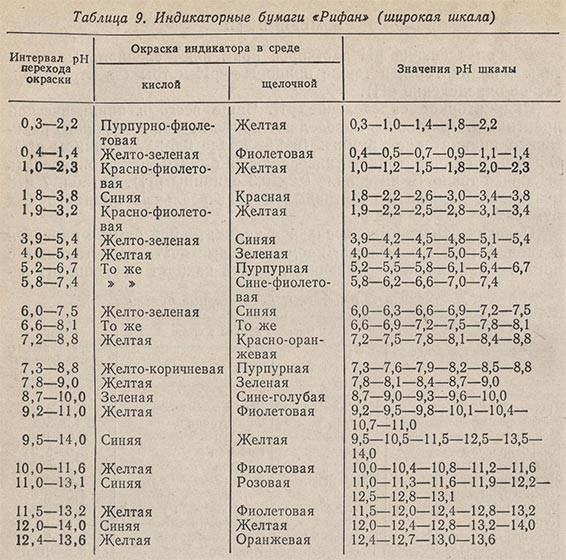
Переход окраски универсальной индикаторной бумаги приведен в табл. 8 и 9. Полученные промежуточные цвета сопоставляют с прилагаемой шкалой сравнения и по ней находят значения pH испытуемого раствора. Индикаторные бумаги можно использовать для определения pH водных растворов с невысокой концентрацией солей и в отсутствие сильных окислителей. Определив pH с помощью универсальной индикаторной бумаги с интервалом pH = 1,0-11,0 или 0-12, уточняют полученный результат с помощью бумаги «Рифан» с более узким интервалом pH.
Электрометрическое измерение pH. Этот метод удобен для измерения pH цветных растворов, в которых индикаторное определение pH (пш) практически невозможно. Для измерений используют приборы – pH-метры со стеклянным электродом, которым обычно заменяют водородный электрод. Очень редко для этой цели применяют сурьмяный или хингидронный электрод.
Стеклянные электроды применяют для определения pH растворов, содержащих тяжелые металлы, окислители и восстановители, а также коллоидных растворов и эмульсий. Определение pH со стеклянным электродом основано на изменении э.д.с. элемента, обратимого относительно ионов водорода.
Потенциал поверхности стекла, соприкасающегося с раствором кислоты, зависит от pH раствора. Это свойство стекла использовано в стеклянных электродах – индикаторах pH. Стеклянный электрод обычно имеет форму пробирки, донная часть которой выполнена в виде тонкостенной стеклянной пластинки или в виде шарика с толщиной стенок не более 0,01 мм. В стеклянный электрод наливают буферный раствор с известным pH и помещают в исследуемый раствор.
В качестве электрода сравнения используют каломельный электрод. Этот электрод представляет собой сосуд, на дне которого находится ртуть, соединенная с цепью платиновой проволокой. Над ртутью находится каломельная паста с кристаллами KCl, сверху насыщенные растворы KCl и каломели (Hg2Cl2). Контакт электрода с исследуемым раствором происходит через тонкое асбестовое волокно. Каломельный электрод сравнения можно применять для измерений pH при температуре не выше 60 °С; нельзя измерять pH растворов, содержащих фториды.
Прибор pH-метр проверяют и настраивают всегда по тому буферному раствору, pH которого близок к pH исследуемого раствора. Например, для измерения pH в области от 2 до 6 готовят буферный раствор по Зеренсену с pH = 3 или 4 или применяют стандартный буферный раствор с pH = 4,62.
В лабораторной практике для измерения pH применяют pH-метр ЛПУ-01, который предназначен для определения pH растворов в пределах от -2 до 14 с диапазоном через 4 единицы pH: -2-2; 2-4; 6-10; 10-14. Чувствительность прибора – 0,01 pH. Используют также pH-метр лабораторный специальный ЛПС-02; pH-метр типа ПЛ-У1 и переносной pH-метр-милливольтметр ППМ-03М1.
Промышленным преобразователем повышенной точности является pH-метр типа pH-261, который предназначается для измерений pH растворов и пульп. В полевых условиях для измерений pH водных растворов применяют pH-метр pH-47М; для измерений pH солевых почвенных вытяжек – pH-метр ПЛП-64; для молока и молочных продуктов применяют pH-метр pH-222-2. Работа на pH-метрах осуществляется согласно инструкции, прилагаемой к каждому прибору.
Вариант №3: Дезинфекция кислородом в таблетках
— После проведения ударного хлорирования средством «Антихлор» снизьте уровень хлора до 0,1-0,3 из расчета, что для снижения уровня хлора на 1 мл/дм3 потребуется 10 грамм на 10м3 воды;
— Корректируем рН при помощи средств рН-минус жидкий из расчёта 100 мл на 10 м3 воды в бассейна для изменения уровня на 0,1 или рН-минус в гранулах из расчёта 75 гр на 10 м3 воды бассейна для изменения на 0,1 и рН-плюс жидкий из расчета 125 мл на 10 м3 воды, чтобы повысить на 0,1 или рН-плюс в гранулах из расчета 100 г на 10м3 воды, чтобы повысить на 0,1. Средство в гранулах предварительно разводят в воде и потом добавляют в бассейн выливая его в чашу по периметру.

— Используйте одну быстрорастворимую таблетку средства «Аквабланк» 200 грамм на 20 м3 воды для шоковой дезинфекции воды, измерьте уровень кислорода специальным «Пултестером О2», когда содержание кислорода будет в пределах 3-5 мг/дм3 бассейн можно использовать для купания;
— Через неделю требуется проверить уровень кислорода в воде, если уровень кислорода ниже 3 мг/дм3, требуется добавить 1 быстрорастворимую таблетку средства «Аквабланк» в 200 грамм на 20 м3 воды;
— Добавляйте средство против водорослей «Альгицид непенящийся» из расчета 100 мл на 10м3 воды бассейна каждую неделю;
— 1 раз в 45 дней проведите шоковую обработку средством «Быстрый хлор в гранулах (БСХ)», в результате которого уровень хлора должен подняться не менее 5 гр/дм3, для этого добавьте 200 гр на 10 м3 воды средства предварительно растворив его в воде в чашу бассейна, выливая его по периметру. Через 24 часа после шоковой дезинфекции проведите дехлорирование воды средством «Антихлор» из расчета, что для снижения уровня хлора на 1 мл/дм3 потребуется 10 грамм на 10м3 воды;

— Проверяйте уровень рН за 12 часов перед купанием, но не реже 1 раза в неделю, корректируйте при необходимости, при добавлении средства в воду перерыв до купающихся должен быть не менее 12 часов.
Щелочная моча
Проблема также может возникнуть, если моча имеет pH выше 7. Результат мочи 8, конечно, все еще является значением в пределах нормального диапазона, и, как уже упоминалось ранее, это значение также не должно означать ничего серьезного. Влияние вегетарианской диеты также может привести к этому значению в общем исследовании. Однако обычно значительная щелочность мочи, то есть pH между pH 7 и 8, позволяет предположить или просто подтвердить (с дополнительными параметрами, например, анализом осадка мочи) об инфекции мочевыделительной системы.
Щелочной pH, помимо инфекций мочевыводящих путей, заболеваний почек или диеты, богатой калием (гиперкалиемия), также является показанием для тестов на работу паращитовидных желез и, опять же, дыхательной системы. Хотя повышенная кислотность мочи может быть вызвана эмфиземой, чрезмерное повышение pH, то есть повышение щелочности мочи, иногда является симптомом астмы.
Один параметр и множество различных интерпретаций помогают в диагностике и лечении заболеваний, связанных не только с выделительной системой. Анализ мочи — это не только анализ, проводимый при подозрении на заболевания или инфекции мочевыделительной системы. Он дает общее представление о состоянии здоровья, и простое изменение pH может помочь определить, в чем проблема.
Можно ли обойтись без определения состава воды?
Ответ здесь однозначный – да! Возможно, опытные владельцы бассейнов сейчас возмутятся, но позвольте объяснить все детальнее.
Бассейны бывают абсолютно разными и по объемам, и по формам, и по материалам, из которых они сделаны. И если у вас небольшой детский бассейн, который устанавливается максимум на 1-2 дня, то химические добавки вам вовсе не пригодятся. Поэтому и замерять вам ничего не придется.
 Детский бассейн может обходиться без химии
Детский бассейн может обходиться без химии
Когда речь идет о стационарных чашах, вода в которых стоит минимум пару недель, то стоит вспомнить и о тестерах для бассейна, и о добавлении химических препаратов. Если вы не будете за ним следить, то за пару дней в нем поселятся микробы, а через неделю все зарастет водорослями.
Надеемся, теперь вы понимаете, почему на главный вопрос наш ответ был положительным. Без специальных тестеров возможно обслуживание самых небольших детских бассейнов, с коротким сроком установки. За этот срок бактерии просто не успеют заселиться и размножиться, так как эту воду вы сольете через пару часов.
Слегка низкий или слегка повышенный pH мочи
Однако иногда при проверке pH мочи при общем осмотре выясняется, что pH повышен. Как правило, небольшие изменения, такие как pH мочи 7 или pH 6, являются стандартными и в большинстве случаев не указывают на какую-либо угрозу здоровью. Такие небольшие изменения могут быть результатом недостаточного или чрезмерного увлажнения тела. Еще одно объяснение — ежедневный рацион.
Люди, которые едят больше продуктов животного происхождения, обычно имеют кислый pH мочи. Вегетарианцы будут иметь щелочной pH мочи. Ни в том, ни в другом случае это не особо опасный показатель. Но следует помнить, что лучше всего, если диета будет разнообразной и не вызывает отклонений ни в одном из параметров нашего тела.
ТОП профессиональных средств
Существует большое количество профессиональных средств, позволяющих удерживать уровень рН воды в искусственных водоемах и бассейнах под контролем.
Измерение

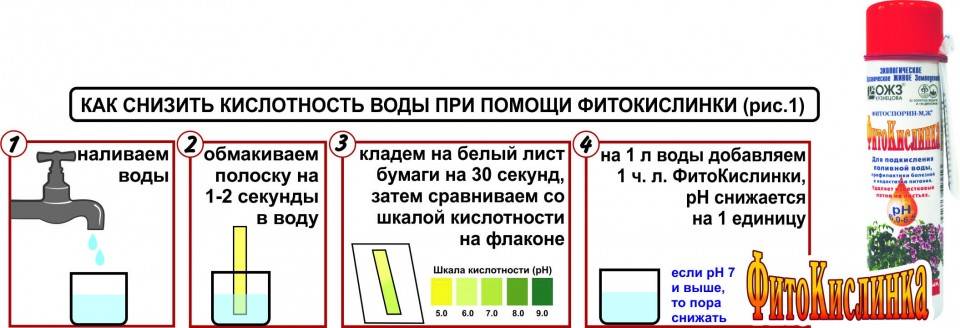
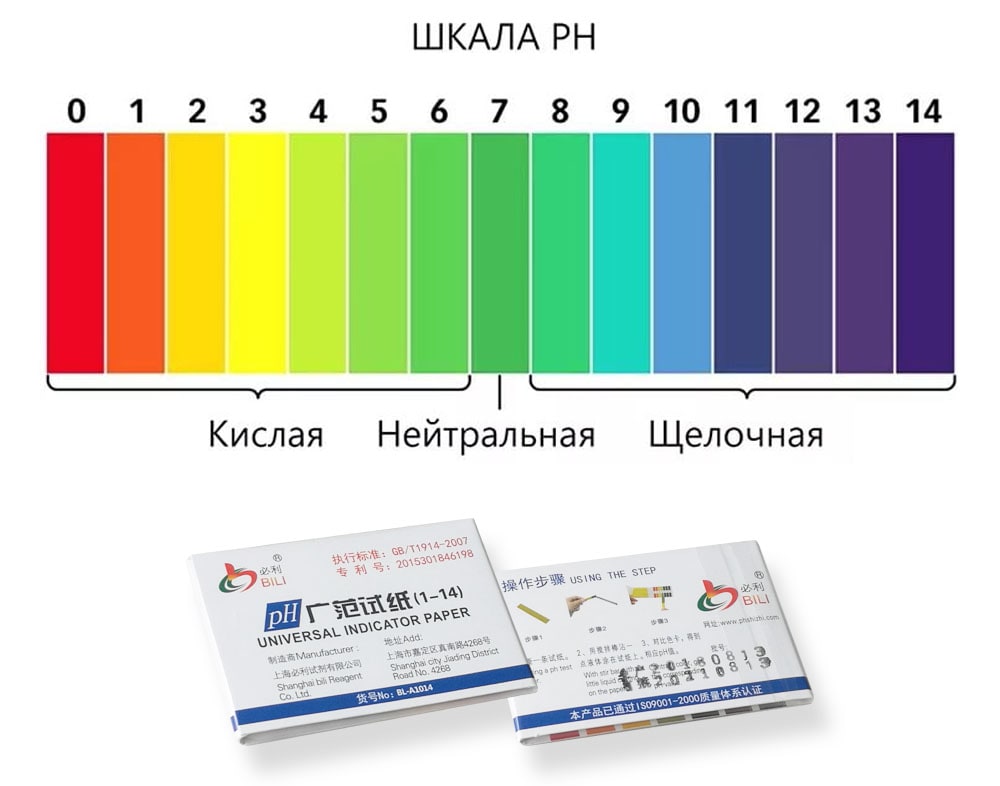
можно воспользоваться лакмусовыми индикаторными бумажками
Узкие полоски бумаги, более чем наполовину пропитанные лакмусом — специальным химически активным веществом, меняющим свою окраску при контакте со щелочной или кислой средой.
Бумажки нижним концом просто окунают в воду, взятую из бассейна, а затем сравнивают проявившийся цвет с таблицей показателей рН (на упаковке).
Простейший метод измерения, но не отличающийся особой точностью. Несомненным плюсом является демократичная цена — набор из 80-150 индикаторных полосок стоит порядка 90-500 рублей.
Наибольшей востребованностью пользуются такие индикаторные лакмусовые наборы:
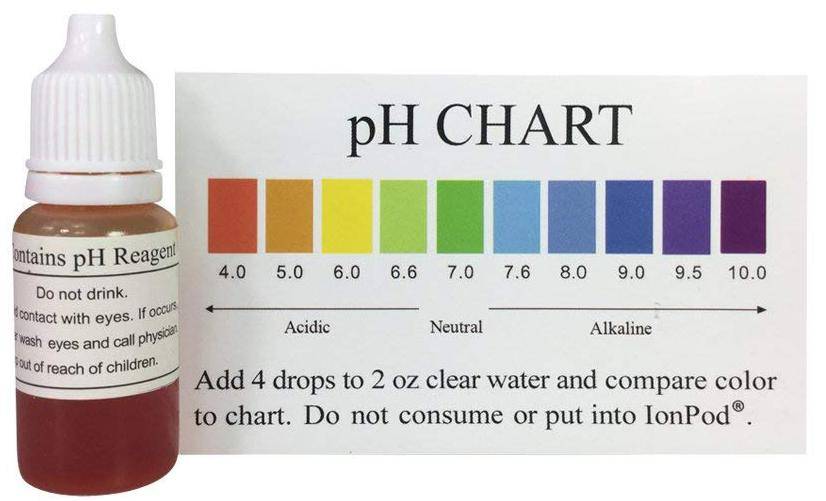
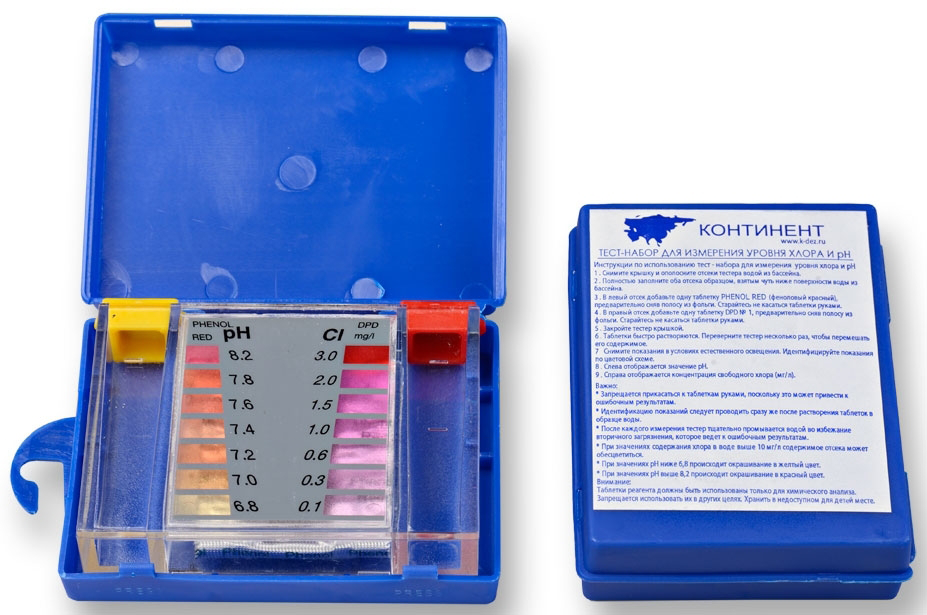
Можно воспользоваться тестерными таблетками. Сухое индикаторное вещество, таблетированное вместе с нейтральным наполнителем, при растворении в проверяемой водной среде изменяющее ее цвет.
Очень наглядный тест, но точных результатов не дающий. Пробу воды из бассейна наливают в специальную мензурку, затем туда же бросают таблетку.
Когда она растворится полностью, а содержимое окрасится, получившийся оттенок сравнивают с цветовой шкалой, имеющейся в комплекте. Примерная стоимость — 150-200 рублей за 10 штук.
Как правило, продаются наборы таблеток для замера сразу нескольких характеристик воды в бассейне:
Однако гораздо сподручнее пользоваться приборами рН-метрами. Различные электронные устройства, практически моментально выдающие измеренное значение на экран с довольно высокой точностью (до 0,1 единицы).
В чистую колбу наливают примерно 30-40 мл воды из бассейна. Затем опускают туда щуп датчика, не забыв предварительно прополоскать его в очищенной дистиллированной воде.
Этот способ требует наличия хотя бы минимальных навыков и умений работы с подобным оборудованием, потому как необходимо регулярно проводить корректировки (иначе точность падает).
Цена немаленькая — приблизительно 1000-5000 рублей (в зависимости от производителя и набора функций).
Среди бюджетных анализаторов выделяют:
По результатам произведенных замеров необходимо произвести соответствующие корректировки с применением специальных средств.
Эти вещества, вступая в химические реакции с агрессивными кислотными или щелочными компонентами, нейтрализуют их и выводят рН воды в бассейне на нужный уровень.
Повышение
Если водная среда в исследуемом бассейне кислая, то для поднятия водородного показателя используют препараты по уходу за водой с пометкой «рН-плюс».
При их изготовлении используется карбонат натрия и бикарбонат натрия или другие щелочи неорганического происхождения.
Чаще всего владельцы бассейнов останавливают свой выбор на следующих средствах рН+:
Понижение
Повышенная щелочная водная среда, что случается в бассейнах гораздо чаще, обязывает применять вещества для коррекции кислотности из серии «рН-минус».
Чаще всего они изготовлены на основе гидрогена сульфата натрия (гидросульфата натрия) или натуральных органических кислот.
Выбор средств рН- намного шире, среди них можно выделить:
Щелочная вода: сода, нашатырный спирт, яичная скорлупа
Чтобы искусственно повысит РН питьевой воды, можно воспользоваться подручными средствами, которые, как правило, имеются в любом доме.
Способ первый: как сделать щелочную воду при помощи нашатырного спирта:
В воду надо добавить нашатырный спирт (на 10 литров берут одну или две капли спирта). Затем желательно измерить РН полученной воды, если она будет приближаться к 14, то воду следует прокипятить.
Способ второй: получаем щелочную воду с помощью пищевой соды.
- вода питьевая – 1 литр;
- сода пищевая – 0,5 ложки (чайной);
- соль пищевая – 0,5 ложки (чайной);
- сахарный песок – по вкусу.
В воде растворить соду и соль, можно добавить немного сахара (для улучшения вкуса).
Полученный раствор перелить в бутылку и хорошенько взболтать. Щелочная вода готова к употреблению.
Способ третий: как сделать щелочную воду для питья старинным способом:
В древности воду ощелачивали с помощью золы. Для этого её надо насыпать в холщёвый мешочек. Затем промыть золу в мешочке под струёй воды и положить в ёмкость с водой для приготовления нужного раствора.
Также для получения щелочной воды использовали измельчённую яичную скорлупу, которую сначала тщательно мыли, затем измельчали в пыль. Воду на скорлупе следовало настаивать примерно сутки.

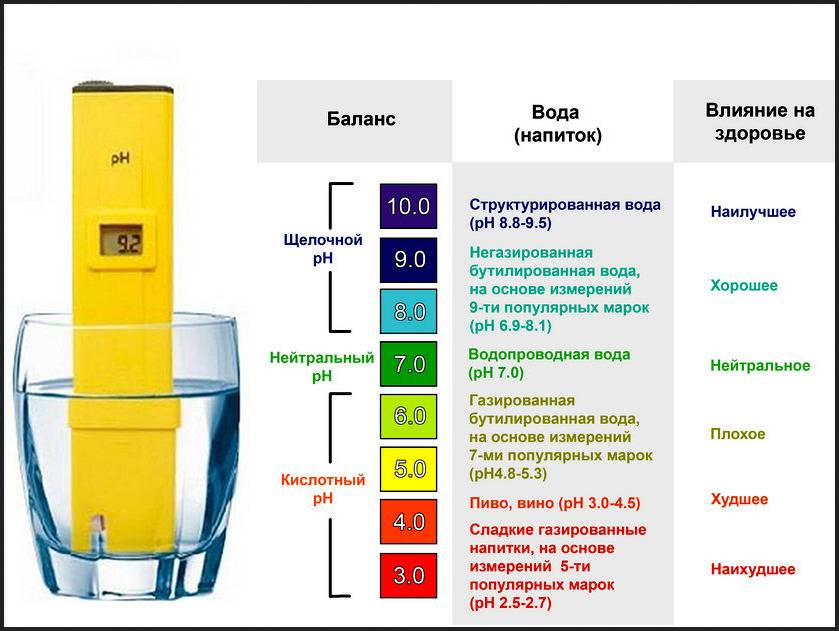
Измерение водородного показателя
Формулы для расчета pH зависят от того, к какому классу относится химическое вещество, входящее в исследуемый раствор, и приведены в специальных справочниках. Более точное значение получают другими методами. Цели и условия проведения исследований определяют, как будет измеряться водородный показатель.
Индикаторные способы
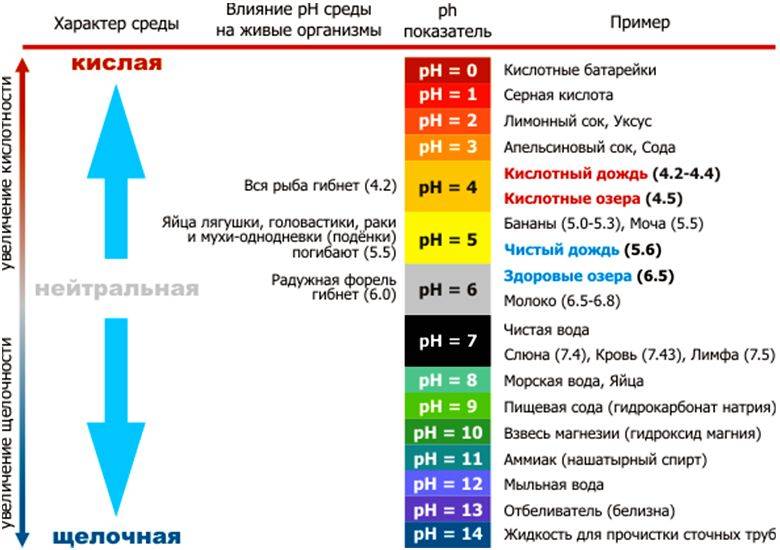
Приблизительно оценить меру активности ионов водорода можно с помощью кислотно-основных индикаторов. Такие вещества обычно относятся к органическим соединениям и имеют свойство изменять свой цвет в разных средах:
- Лакмус меняет цвет от красного в кислой среде через фиолетовый в нейтральной до синего в щелочной.
- Фенолфталеин становится синим в щелочной среде, оставаясь бесцветным в остальных.
- Метилоранж розового цвета соответствует повышенной кислотности, оранжевого — показывает нейтральность среды, в щелочах становится синим.
Изменение происходит для каждого индикатора в своём диапазоне кислотности, обычно составляющем 1—2 единицы. При этом методе результат можно получить быстрый и наглядный при небольших затратах, но недостаточно точный, с большой погрешностью при исследовании очень слабых растворов, окрашенных или мутных вод. Используется, когда нужно найти предварительное определение pH.
Более широкий диапазон и выше точность у универсального индикатора. Он соединяет в себе несколько индикаторов и градуируется в соответствии со значениями pH от единицы до десяти. Соответствие значения водородного показателя и цвета:
- 1 — красный;
- 2 — розовато-оранжевый;
- 3 — оранжевый;
- 4 — темно-желтый;
- 5 — желтый;
- 6 — желтовато-зеленый;
- 7 — светло-зеленый;
- 8 — насыщенный зеленый;
- 9 — сине-зеленый;
- 10 — сине-серый.
Аналитический объемный метод
Кислотно-основное титрирование — метод определения водородного показателя среды с помощью так называемых титрантов. В основном для этого используются сильные кислоты (серная, соляная) и сильные щелочи (едкий калий, каустическая сода).
Раствор-титрант добавляют в исследуемую жидкость по каплям. При этом они вступают в химическую реакцию. Когда она завершается, наступает точка эквивалентности, т. е. момент отчетливого изменения окраски исследуемого раствора. По установленному в результате опыта объему титранта, необходимому для получения точки эквивалентности, и известному значению его концентрации можно рассчитать pH с высокой точностью.
Измерительный прибор pH-метр
Ионометрический метод, при котором кислотный показатель можно измерить с помощью специализированного прибора — pH-метра, является наиболее точным (до сотых от единицы pH), удобным и имеет широкий диапазон измерения. PH-метр представляет собой милливольтметр, способный измерять разность потенциалов со стеклянных электродов. У него также есть система пересчета напряжения в pH.
В исследуемый раствор погружают индикаторный электрод и электрод сравнения, замыкая таким образом гальваническую цепь. Величина электродвижущей силы в ней зависит от активности ионов H+ в растворе, т. е. является функцией только его pH. Индикаторный электрод состоит из стеклянной трубки, заполненной специальной суспензией в растворе соляной кислоты, и погруженной в нее серебряной проволоки.
Специализированный прибор, применяемый в медицине для исследований pH жидкостей желудочно-кишечного тракта, называется ацидогастрометром. Включает в себя регистрирующий блок и один или несколько зондов. Для измерения уровня pH таких биологических жидкостей, как слюна и моча, применяются электронные pH-метры.
Этап 2: Корректируем рН
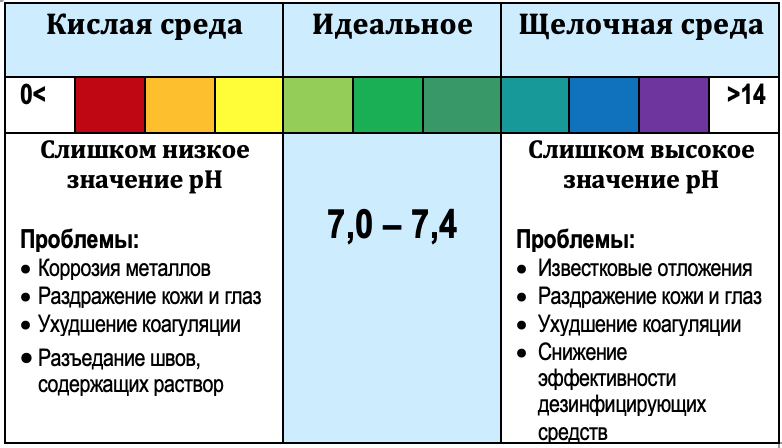
Нормальный уровень 7,2-7,6, при первом запуске рекомендуем довести уровень рН до 7,2, так как при добавлении хлора рН будет повышаться.
— корректируем рН при помощи средств рН-минус жидкий (из расчёта 100 мл на 10 м3 воды в бассейна для изменения уровня на 0,1) или рН-минус в гранулах (из расчёта 75 гр на 10 м3 воды бассена для изменения на 0,1) и рН-плюс жидкий (125 мл на 10 м3 воды, чтобы повысить на 0,1) или рН-плюс в гранулах (100 г на 10м3 воды, чтобы повысить на 0,1). Сухое средств предварительно разводят в воде и добавляют в бассейн.
— включаем фильтрацию, ждем 12 часов, когда средство полностью сработает
— измеряем рН в воде в бассейна профессиональным «Пултестером Lovibond» или «Тестовыми полосками».


Способы понижения pH в аквариуме
Если кислотно-щелочной баланс чересчур высок, нужно его снизить. Для этого можно использовать покупные средства или воспользоваться народными методами.

Магазинными средствами
Уменьшить pH в вашем аквариуме можно покупными препаратами, в составе которых есть фосфорная кислота. Однако переусердствовать не стоит – это вещество способствует бурному росту растительности. Понижать кислотность также можно препаратами, содержащими в составе дубовую кору и ольховые соцветия.
Народные способы
Для снижения кислотности можете попробовать метод вымораживания:
- Налейте воду в таз и оставьте емкость в холодном месте.
- После замерзания жидкости наполовину, пробейте лед.
- Удалите лишнюю воду, а лед растопите, после чего добавьте полученную жидкость в аквариум.
Есть и другой хороший вариант, в котором основным компонентом будет торф:
- Залейте пять граммов торфа литром очищенной воды.
- На протяжении одного дня проверяйте кислотность: если она останется высокой, процедите раствор и потихоньку добавьте его в аквариум.
Разновидности кислотно-щелочного дисбаланса
Кислотно-щелочной дисбаланс может проявляться в виде алкалоза – когда повышается количество щелочных веществ в жидкостях, или ацидоза – когда повышается уровень кислот. В свою очередь эти процессы могут проявляться как:
- метаболический ацидоз;
- респираторный ацидоз;
- метаболический алкалоз;
- респираторный алкалоз.
Метаболический ацидоз
Метаболический ацидоз может быть вызван острыми метаболическими нарушениями, возникающими при некоторых инфекционных заболеваниях и критических состояниях. Хронический метаболический ацидоз обычно развивается незаметно в течение многих лет. Бывает у людей, страдающих сахарным диабетом, заболеваниями почек.
К повышенной выработке в организме кислот приводят следующие факторы:
- злоупотребление пищей, богатой животными белками;
- чрезмерные физические нагрузки;
- стресс;
- воспалительные процессы;
- соблюдение низкоуглеводной диеты.
Сами по себе эти факторы не являются опасными для человека, но если они сохраняются длительно, риск ацидоза повышается.
Признаки метаболического ацидоза довольно расплывчаты и неспецифичны. Они могут включать такие симптомы как хроническая усталость, слабость, снижение массы и плотности костной ткани, а также проблемы с кожей, ногтями и пищеварением. Нарушение кислотно-щелочного баланса в сторону повышения кислотности также может повлиять на функционирование периферической и центральной нервной системы, вызывая «затуманенность» мозга, беспокойство, мышечные спазмы.
Респираторный ацидоз
Респираторный ацидоз развивается из-за неспособности легких выводить избыток углекислого газа из организма. Во многом признаки нарушения схожи с метаболическим ацидозом.
Эта разновидность кислотно-щелочного дисбаланса может появляться на фоне приема некоторых препаратов, после травмы грудной клетки или обструкции дыхательных путей. Специфический симптом – замедленное и поверхностное дыхание больного.
Причины ацидоза
Кислотно-щелочной дисбаланс, проявляющийся ацидозом, может появляться в силу разных факторов и нести с собой опасные клинические последствия. Как правило, кислотность организма повышается в результате нарушения работы органов, призванных регулировать pH. Чаще всего такое случается на фоне некоторых заболеваний, таких как:
- почечная недостаточность;
- нарушение дыхательной функции, например, при хронической обструктивной болезни легких или сердечной недостаточности;
- сахарный диабет, при котором развивается кетоацидоз;
- хроническая диарея;
- гипоксия, в ходе которой развивается лактоацидоз;
- отравление алкоголем, салицилатами, этиленгликолем.
Метаболический алкалоз
Об этом состоянии говорят, когда в силу определенных метаболических процессов в организме сильно повышается содержание бикарбоната (щелочей).
Такое состояние обычно связывают с передозировкой бикарбоната натрия, употреблением наркотиков, сильным обезвоживанием, вызванным в том числе продолжительной рвотой, диареей.
Респираторный алкалоз
Это патологическое повышение в организме щелочей, вызванное усиленным выведением углекислого газа. Респираторный алкалоз может случаться из-за гипервентиляции легких, а также бывает у пациентов после болевого шока. Иногда причиной этого нарушения служат чрезмерная физическая нагрузка, лихорадка, некоторые легочные заболевания (пневмония, бронхит, астма, ХОБЛ). В некоторых случаях может развиться после длительного приема лекарственных препаратов.
Причины алкалоза
Причиной алкалоза чаще всего является дефицит калия и/или водорода. Такое возможно в случае:
- применения глюкокортикостероидов, которые вызывают снижение концентрации калия и повышение натрия в сыворотке крови;
- чрезмерной потери «кислых» ионов водорода (например, в результате продолжительной и сильной рвоты);
- вымывания калия после приема диуретиков;
- гипервентиляции легких, в ходе которой уменьшается концентрация двуокиси углерода, ответственного за «кислотность».
Что влияет на показатель ph
Кислотность воды имеет тесную взаимосвязь с карбонатной жёсткостью (КН) и щелочностью. При повышении рН на одно деление, КН вырастает в 10 раз. Высокая плотность нитратов неизбежно приведёт к понижению щелочности. Когда плотность продолжает увеличиваться, щелочь не сможет удержать уровень водородного показателя, который резко упадёт.
Увеличение кислотности означает повышенный уровень содержания аммиака. Водородные показатели не являются неизменной величиной. За сутки могут меняться несколько раз. В основном, это связано со сменой концентрации углекислоты в водной среде, но есть и другие моменты:
- наличие минеральных веществ;
- температурный режим;
- насыщенность кислородом;
- разновидности грунта;
- удобрения для растений;
- чистота фильтра;
- плотность заселения водными обитателями;
- периодичность чистки грунта;
- материал декораций.
Растения днём потребляют много углекислого газа, это увеличивает рН. Ночью нет процесса фотосинтеза и активная реакция воды низкая. В совокупности все перечисленные факторы имеют большее воздействие на биологический баланс аквариума, чем эффект от концентрации водорода.
Как понизить ph в аквариуме
Понизить уровень ph в аквариуме обычно сложнее, чем повысить. Существуют разные варианты:
- Субстрат торфяного моха. Положить его в бункер фильтра (в сумочке) либо под слой грунта. Каждые полмесяца делают замену, чтобы не допустить его гниения. Торф плавно понижает уровень pH. Требуется проследить, чтобы торф, подложенный под грунт, не загнивал.
- Отвар торфа. Кипятят продукт в дистилляте 30 минут (5 г на 1 литр). Вода окрасится в темно-коричневый цвет. Отвар процеживают и выливают в аквариум малыми партиями, распределяя его равномерно по всему резервуару.
- Экстракт торфа. Препарат на базе вытяжки торфа, в котором находятся танин, гуминовые кислоты и гормоны. Использование экстракта благотворно сказывается на рыбах, улучшает рост растений, действует как природный антисептик. Целесообразно применять этот метод снижения кислотности экстрактом торфа, когда аквариум заселён сложными в уходе, редкими породами рыб.
- Коряги. С помощью многих видов древесины можно снизить рН. Дубильные вещества играют роль окислителей. Корягу промывают и используют как элемент интерьера. Для водных обитателей этот способ хорош тем, что уменьшить уровень кислотности получается медленно и незаметно.
- Чёрный чай. Действующими элементами чая являются дубильные вещества, аминокислоты и алкалоиды. Необходимо заварить в отдельной посуде концентрированный чай. Добавлять порциями, измеряя ph.