Использует
Ядерный магнитный резонанс
Оксид дейтерия используется в спектроскопии методом ядерного магнитного резонанса (ЯМР). Действительно, поскольку резонансная частота дейтерия отличается от резонансной частоты обычного протона, этот растворитель не мешает измерению.
Нейтронный замедлитель
Тяжелая вода используется в некоторых секторах в ядерных реакторах в качестве замедлителя нейтронов для того , чтобы замедлить нейтроны от реакции ядерного деления . Таким образом, замедленные нейтроны с большей вероятностью вызовут новые деления ядер урана , что приведет к цепной реакции .
В различных типах ядерных реакторов используется с водой под давлением в умеренных количествах с тяжелой водой:
- Canadian- разработан реактор CANDU и его производные;
- два реактора с тяжелой водой под давлением (PHWR) атомной электростанции Atucha ( Аргентина ) немецкой конструкции Siemens / Kraftwerk Union .
«Классическая» вода (H 2 O) также может замедлять нейтроны в реакции деления, но поглощает слишком много из них, чтобы реакция могла быть самоподдерживающейся в реакторе на природном уране. Поэтому его можно использовать только с реакторами, в которых используется обогащенный уран .
Детектор нейтрино
Нейтринная обсерватория Садбери , SNO (Онтарио, Канада ), использует 1000 тонн тяжелой воды в бачке захоронен в шахте более двух километров под землей , чтобы защитить от космических лучей . SNO обнаруживает эффект Черенкова, возникающий при взаимодействии нейтрино с тяжелой водой.
Топливный цикл
Стандартно AHWR настроен на закрытый ядерный топливный цикл потому что это приведет к снижению радиотоксичности. Из-за этого у AHWR есть альтернативные варианты топлива, учитывая, что он имеет различные топливные циклы. Он может выполнять замкнутые и прямоточные топливные циклы. Общий вид AHWR рассчитан на сильное выгорание с торий -основное топливо (BARC, 2013). Рециклированный торий, извлеченный из реактора, затем отправляется обратно, и плутоний хранится для последующего использования в . Топливо для AHWR будет производиться ADVANCED FUEL FABRICATION FABRICATION FACILITY, которое находится под руководством BARC Tarapur. В настоящее время AFFF работает над производством твэлов PFBR. В прошлом AFFF был связан с производством топливных стержней для других исследовательских целей. AFFF – единственное предприятие по производству ядерного топлива в мире, которое имеет дело с ураном, плутонием и торием.
И еще несколько уникальных возможностей
Оксид водорода в нормальных условиях (при определенных показателях температуры и давления) – это бесцветная жидкость без вкуса и запаха. Но, оказывается, в таких обстоятельствах сохранять текучесть способна только вода. В аналогичной ситуации другие похожие соединения водорода предстают перед человеком в виде газов. Такие качества снова обусловлены специфическими связями внутри молекулы Н2О.
Если опрокинуть стакан, то содержимое не разлетается по сторонам, не рассыпается, а образует лужу с четко очерченными краями. Это происходит благодаря специфике молекулы воды – субстанция сохраняет вязкость и высокое поверхностное натяжение (по этому показателю монооксид дигидрогена проигрывает только ртути).
Оксид водорода является одним из лучших веществ-растворителей. Избегая научной терминологии, этот процесс можно описать примерно так. Молекулы воды берут в кольцо каждую молекулу растворенного вещества. Но не хаотично, а по определенной схеме: ионы с положительным зарядом притягивают к себе атомы кислорода, а отрицательно заряженные частицы – водород. По такому же принципу вода заполняет пространство в клетках всех живых организмов.
Поскольку в воде почти всегда есть какие-либо соли, то есть присутствуют ионы с положительным и отрицательным зарядом, она также обладает способностью электропроводности. При этом чистая вода, не содержащая в себе примесей других ионов, наоборот является идеальным изолятором.
Что такое гидросфера
Гидросфера представляет собой водную оболочку Земли, расположенную между атмосферой (газовой оболочкой) и литосферой (твердой земной корой).
В состав гидросферы входит вода, которая представлена в 3 состояниях:
- жидком,
- твердом (ледники),
- газообразном (в виде водяного пара, входящего в состав нижних участков атмосферы).
В состав данной системы входит большое количество различных химических элементов: различных минеральных солей, газов, других соединений.
Гидросфера является динамической, постоянно меняющейся системой, образующей круговорот воды в природе, когда жидкость испаряется из источников, поднимаясь в виде газа в атмосферу, а затем конденсируется, выпадая в виде осадков.

Теории формирования
В современном научном обществе существуют 2 основных теории формирования гидросферы.
Это:
- теллурическая теория,
- космическая теория.
Приверженцы теллурической теории считают, что земная кора, атмосфера и водная оболочка планеты формировались в одно и то же время, разделяясь в результате процессов плавления и высвобождения газов, запертых в твердых веществах.
Известно, что Земля сформировалась из протопланетного облака, в составе которого уже находились различные элементы, но они входили в состав твердых частиц. Когда планета достигла довольно большого размера, в ней стали происходить определенные изменения, которые связаны с силами гравитации и распадом радиоактивных элементов в недрах Земли. Все это привело к разогреву планеты, что в свою очередь стало причиной дифференциации ее составных элементов.
Самые легкие из них, постепенно превращаясь в пар, сформировали основу атмосферы, а затем и гидросферы, более тяжелые вошли в состав земной коры и недр планеты (наиболее объемные элементы, например железо и никель, составляют земное ядро и мантию).
Водная оболочка Земли формировалась очень медленными темпами. Сначала все легкие элементы преобладали в газообразном состоянии, но благодаря тому, что температура над поверхностью планеты была сравнительно невысокой (по сравнению с ее недрами), эти газы конденсировались, образуя с течением времени гидросферу.

Космическая теория гласит, что вся вода, которая содержится на нашей планете, имеет внеземное происхождение. Она была доставлена кометами и метеорами, прилетающими из космоса. В тот период времени, когда планета только сформировалась, она подвергалась постоянным ударам космических тел, в состав которых входили мельчайшие частички воды. Конечно, их количество было весьма незначительным, но благодаря тому, что эта атака продолжалась на протяжении миллионов лет, на поверхности и в недрах планеты скопились масштабные водные запасы.
Существует мнение, что обе этих теории являются верными. Согласно этому мнению, часть гидросферы сформировалась в результате естественных планетарных процессов, характерных для планет земного типа, другая часть прибыла к нам вместе с космическими телами.

Что такое тяжелая вода?
Чтобы разгадать тайну тяжелой воды, нужно сначала понять концепцию изотопов. Когда атомы элемента отличаются числом нейтронов в их ядре, они известны как изотопы. Водород имеет следующие изотопы.
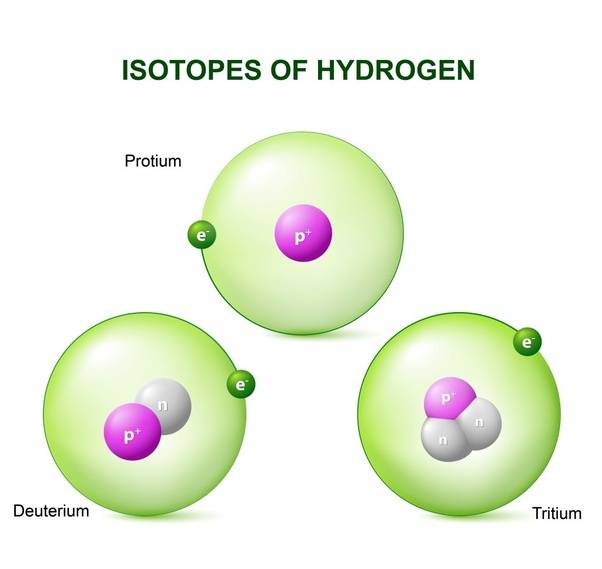 Изображение протия, дейтерия и трития
Изображение протия, дейтерия и трития
Дейтерий — это изотоп водорода, который содержит на один нейтрон больше, чем стандартный атом водорода. Из-за этого дополнительного нейтрона в каждом атоме дейтерия, он по существу весит вдвое больше, чем у нормального атома водорода.
Подобно химической структуре воды (H 2 O), тяжелая вода или оксид дейтерия (D 2 O) также имеют два атома, связанных с одним атомом воды. Вместо обычных атомов протия тяжелая вода состоит из двух атомов дейтерия.
Как и обычная вода, тяжелая вода — это жидкость не имеет запаха при комнатной температуре. Более того, дейтерий, равный протию, также является стабильным изотопом. Это гарантирует, что тяжелая вода не радиоактивна. Молекулярный вес каждого атома дейтерия равен 20, тогда как вес атома H 2 O имеет молекулярный вес всего 18. Из-за более высокого веса дейтерий более плотный, чем вода. В твердом состоянии блок D 2 O будет тонуть в воде, а не плавать.
 Молекулярная структура D2O
Молекулярная структура D2O
Это отличается от того, как ведет себя кусок льда (H 2 O). Простой способ различить D 2 O и H 2 O — это вес и плотность двух соединений. Тяжелая вода встречается в природе, но не так часто, как вода. Соотношение встречающейся в природе тяжелой воды и обычной воды составляет где-то 1: 20 000 000 молекул.
Фон
Центр атомных исследований Бхабхи (BARC) создала крупную инфраструктуру для облегчения проектирования и разработки этих усовершенствованных тяжеловодных реакторов. В нее следует включить такие аспекты, как технологии материалов, критические компоненты, физика реактора и анализ безопасности. Для экспериментов с этими реакторами было создано несколько установок. AHWR – это тяжеловодный реактор с трубчатым давлением. Правительство Индии, Департамент атомной энергии (DAE) полностью финансирует будущую разработку, текущую разработку и проектирование усовершенствованного тяжеловодного реактора. Новая версия Advanced Heavy Water Reactors будет оснащена более общими требованиями безопасности. Индия является базой для этих реакторов из-за больших запасов тория в Индии; поэтому он больше приспособлен для непрерывного использования и работы с AHWR.
Химический реактор
Реактор — устройство, действующее на основе различных типов реакций (физических, химических, биологических и т. п.)
Химический реактор или как его ещё называют Реактор химического синтеза — агрегат для проведения химических реакций объёмом от нескольких миллилитров до десятков и сотен кубометров.
В зависимости от условий протекания реакций и технологических требований реакторы делятся: реакторы для реакций в гомогенных системах и в гетерогенных системах; реакторы низкого, среднего и высокого давления; реакторы низкотемпературные и высокотемпературные; реакторы периодического, полунепрерывного и непрерывного действия.
Цель работы химического реактора – выработка конечного продукта из исходных компонентов при соблюдении требований максимальной эффективности процесса:
Создание устойчивого и стабильного режима проведения реакции;высокие энергетические показатели; минимальная стоимость реактора; простота работы и ремонта.
Процессы, протекающие в химических реакторах, могут быть описаны в рамках нескольких идеальных моделей:
Идеального смешения, где концентрация целевого продукта мгновенно скачкообразно меняется от начальной до установившейся в реакторе;Идеального вытеснения, где движущийся поток можно представить в виде нескольких несмешивающихся друг с другом объемов и характер движения их поршнеобразный;Однопараметрическая диффузионная модель – допускается, что в потоке имеет место только продольная диффузия;Ячеечная модель – поток представляется в виде совокупности ячеек, в каждой из которых происходит идеальное смешение, а между ними массообмен отсутствует.
Химические реакторы внутренним объёмом до 10 литров применяются в основном в лабораториях в исследовательских целях и в пилотных установках.
Реакторы объемом от 100 литров работают в химической, фармацевтической, целлюлозной, парфюмерной промышленности и других.
Химические реакторы используются для ведения различных химических реакций, испарения, кристаллизации, плавления и гомогенизации исходных компонентов или продуктов реакции.
Стеклянный химический реактор широко используется в качестве биохимического инструмента, используется в современных тонких химических, биологических фармацевтических, научно-исследовательских и других отраслей промышленности. Стеклянный реактор химического синтеза – Это идеальный инструмент для обучения, эксперимент, экспериментальные и производственные.
Снабженный защитной оболочкой стеклянный реактор нашел широкое применение для выполнения химических реакций объединения, разделения и концентрации. Различные нагреваемые или охлаждающие жидкости типа воды или масла могут подаваться в меж оболочное пространство снабженного защитной оболочкой стеклянного реактора, обеспечивая поддержание для реакций постоянной температуры. Кроме того, реактор может обеспечивать качественное смешивание реактивов в лабораторном сосуде при атмосферном давлении или в вакууме. Конструкция из прозрачного стекла позволяет следить за ходом реакции.
Лабораторный Химический реактор по мимо защитной оболочки в большинстве случаев имеет или доукомплектовывается Охладителем, Мешалкой, Вакуумным либо мембранным насосом, Рубашкой, Термостатом.
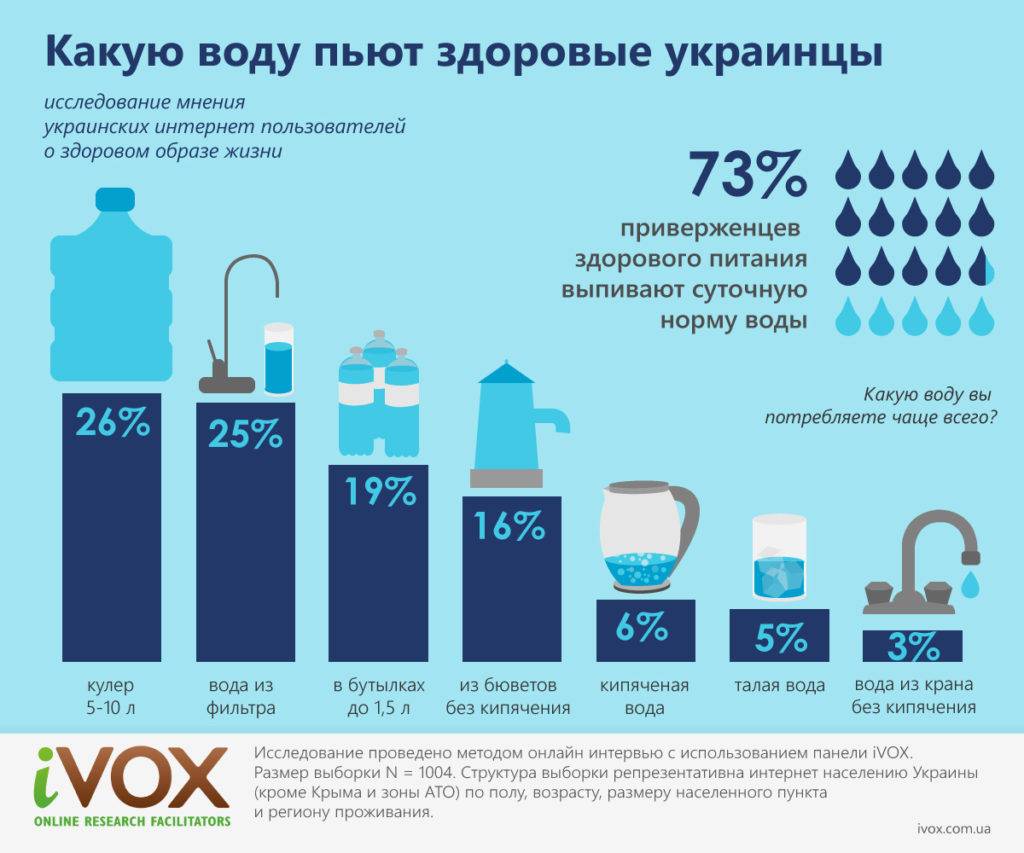
Сколько влаги необходимо человеку
Сколько воды необходимо пить ежедневно? На этот, казалось бы, простой вопрос нет однозначного ответа. На протяжении многих лет ученые проводили много исследований и каждый раз озвучивали разные цифры. На самом деле, единого ответа и не существует. Все зависит от возраста, пола, среды обитания и рода деятельности человека.
Люди, живущие на побережье, получают дополнительную влагу из воздуха, поэтому могут позволить себе выпивать немного меньше жидкости, чем другие. А вот жители жарких стран, наоборот, должны как можно тщательнее контролировать свой водный баланс, так как более подвержены обезвоживанию.
Употребление жидкости в меньшем количестве, чем этого требует организм, ведет к серьезным нарушениям в работе систем и органов. Но избыток также опасен для здоровья. Так кому и сколько воды положено?
При нормальных обстоятельствах количество влаги в организме контролирует жажда и мочеотделение. И это обычный водный цикл. Не стоит забывать, что жажда может быть признаком некоторых болезней, в частности сахарного диабета. Поэтому, если желание пить не пропадает на протяжении долгого времени, нужно не откладывая обратиться к врачу.
В 2010 году на своем очередном съезде диетологи Европы предложили минимальными нормами потребления воды считать:
- 2 л – для мужчин;
- 1,6 л – для женщин.
Но это только приблизительные цифры, которые не учитывают образ жизни и физическую активность человека.
Помимо этого существует формула, по которой можно рассчитать более точную суточную норму, исходя из массы тела. Для этого достаточно знать, что на 1 кг веса должно приходиться по 30 мл воды ежедневно.
Вода спасет от лишних килограммов
Любительницы диет для похудения, скорее всего, знают: бороться с чрезмерным аппетитом помогает вода. Разыгрался голод? Обмануть организм легко. Для этого достаточно выпить стакан теплой воды – желудок растянется, в мозг пойдут сигналы о насыщении.
Кроме того, согласно исследованиям, 500 мл жидкости способны временно (на протяжении 90 минут) ускорять метаболизм на 25-30 %. А выпитые 2 л воды в день, по подсчетам ученых, увеличивают расход энергии примерно на 96 калорий. При этом лучше отдавать предпочтение холодной воде – организм потратит дополнительные калории на согревание жидкости.
Иные исследования показали: стакан воды, выпитый примерно за полчаса до еды, также способен уменьшить количество употребляемых калорий. Особенно эффективно этот прием работает в пожилом организме. Сидящим на диете достаточно выпивать перед едой 2 стакана воды, чтобы за 12 недель сбросить на 44 % больше лишнего веса.
Но на этом влияние воды на вес тела не ограничивается. Дефицит Н2О, наоборот, может послужить причиной ожирения. И все дело в том, что испытывающий жажду организм, пребывая в состоянии стресса, посылает мозгу сигналы… о голоде. Человек принимается кушать, а лишние калории откладываются в виде подкожного жира.
В чем польза для организма
Живая вода обладает множеством полезных свойств:
- устраняет признаки аллергической реакции;
- борется с кожными заболеваниями;
- защищает клетки от воздействия радиации;
- увеличивает ценность экзогенных и эндогенных антиоксидантов;
- выводит из организма шлаки, токсины и тяжелые металлы;
- активирует развитие защитной реакции организма.
При регулярном приеме водородной воды происходит оздоровление всех систем внутренней секреции. Такое питье полезно не только для взрослых людей, но и детей, беременных и кормящих женщин.

При спортивных тренировках
Ощутимую пользу источника долголетия оценят те, кто придерживается здорового образа жизни. Во время занятия спортом человеку требуется значительное количество кислорода. Благодаря употреблению молекулярного водорода можно восстановить водный баланс и вывести излишние оксиданты, накопившиеся при интенсивных физических нагрузках.
Обогащенная молекулами водорода жидкость полезна для спортсмена, хотя бы по причине того, что она способна:
- активировать обменные процессы в организме;
- препятствовать накоплению молочной кислоты в мышцах;
- подавлять развитие патологических процессов;
- снижать риск повреждения мышечной ткани.
 Водород обладает регенерирующимисвойствами и снабжает организмдополнительной энергией
Водород обладает регенерирующимисвойствами и снабжает организмдополнительной энергией
При похудении
При регулярном употреблении молекулярного водорода:
- нормализуется уровень сахара в крови;
- стабилизируется концентрация жировых клеток в печени;
- организм насыщается влагой.
Помимо этого живая вода помогает людям, страдающим от ожирения.
Для снижения веса также отлично подойдут смузи на основе овощей, ягод и фруктов
В косметологии
Водородный напиток оказывает полезное действие не только на органы внутренней секреции. Он производит хороший эффект на кожу и волосы. Утренние умывания живой водой позволяют избавиться от:
- гнойных ранок;
- раздражений;
- покраснений.
Также вещество наделено защитными свойствами, предупреждая негативное воздействие ультрафиолетовых лучей на кожу.
 Напиток способствует разглаживанию морщин
Напиток способствует разглаживанию морщин
Противопоказания к употреблению
Молекулы напитка не представляют опасности для здоровья. Еще с уроков биологии известно, что в кишечнике человека образуется водород. Живая вода не способна сохранять полезные качества длительное время. Водород быстро испаряется, поэтому к приему рекомендуется только свежеприготовленный напиток.
Библиография
- Savard J., ” Электролиз на постоянном уровне смеси легкой и тяжелой воды “, J. Phys. Радий , п о 5 (5)1944 г., стр. 85-89.
- (JA) Oinque Yasusi, « Влияние тяжелой воды для бутона перерыва виноградной лозы , журнал Японского общества садоводства науки , п о 7 (1),1936 г., стр. 207-208 .
- (ru) Кушнер Д.Д., Бейкер А. и Данстолл Т.Г. « Фармакологическое использование и перспективы тяжелой воды и дейтерированных соединений » , Canadian Journal of Physiology and Pharmacology , vol. 77, п о 21999 г., стр. 79–88 .
- Раевский В., “ Переходные режимы в тяжеловодном реакторе ”, J. Phys. Радий , п о 14 (7-9),1953 г., стр. 473-477 .
- Сент-Обен Э., Регулировка механизмов перезагрузки и реактивности реакторов CANDU для усовершенствованных топливных циклов , (докторская диссертация) Политехническая школа Монреаля,2013.
Дейтерированные растворители для ЯМР |
|---|
|
Агрегатные состояния
Из всех веществ, существующих на Земле, только вода может иметь три принципиально разных агрегатных состояния: жидкое, газообразное и твердое. Благодаря трём агрегатным состояниям происходит круговорот воды в природе и жизнь на Земле. Рассмотрим подробнее каждое агрегатное состояние.
- Жидкое (вода). В нормальных условиях вода является жидкостью. Образует мировой океан, реки, ручьи и т.д.
- Газообразное (водяной пар) — это бесцветный газ, не имеет вкуса и запаха. Испаряется с поверхности океанов, рек, болот, почвы, растений и поступает в воздух или образуется путём кипения жидкой воды или сублимации из льда. Сублимация — переход вещества из твёрдого состояния сразу в газообразное, минуя стадию плавления (перехода в жидкое состояние).
- Твердое (лёд). При температуре от нуля и ниже вода превращается в лёд. В холодное время года он сковывает реки и лужи, выпадает в виде осадков: снежинок, града, инея, образует ледяные облака. Встречается в виде ледников и айсбергов.
Строение в различных агрегатных состояниях
Жидкая вода, лёд и водяной пар имеют один и тот же состав, но разные состояния.
Рассмотрим строение молекулы на изображении.
Многочисленные исследования ученых подтверждают, что по структуре вода и лед близки друг к другу. Структура льда – это решетчатый каркас. Структура воды зависит от содержания разных веществ, которые в ней растворяются, а также от нерастворимых соединений и некоторых других факторов.
В воде возникают структуры, которые стали называть «кластерами» — группа атомов или молекул, которые представляют собой единую структуру, но внутри имеют свои индивидуальные особенности.
При температуре близкой к точке замерзания, молекулы жидкой воды собираются в небольшие группы, практически так, как в кристаллах. При температуре близкой к точке кипения они располагаются более свободно.
Свойства
Вода — уникальный природный компонент, который обладает рядом свойств. Рассмотрим основные:
- не имеет цвета, запаха и вкуса;
- распространенный растворитель;
- обладает высоким поверхностным натяжением, уступая в этом только ртути;
- имеет большую теплоту испарения (используется для терморегуляции);
- чистая вода — хороший изолятор;
- обладает большой теплоёмкостью (увеличение тепловой энергии вызывает лишь сравнительно небольшое повышение ее температуры);
- плотность в разных диапазонах температур меняется неодинаково.
Существуют необычные свойства. Например, в твердом виде вода легче, чем в жидком. Лёд не тонет в воде. В твёрдом состоянии частички воды располагаются по порядку, между ними остается много свободного пространства. Когда лёд тает, активность частичек повышается, свободное пространство заполняется. Жидкая форма становится более тяжелой, нежели твердая.
Такая уникальная способность даёт возможность любому водоёму не замерзать по всей глубине. Даже при самом сильном морозе температура воды у дна не опускается ниже +4 ᵒС. Все живые существа (рыбы и другие) могут спокойно пережить самую суровую зиму подо льдом.
Горячая вода замерзает быстрее, чем холодная. Это связано с большей скоростью испарения и излучения тепла.
Теплоемкость и некоторые другие физические свойства воды тоже зависят от температуры неодинаково. Другие виды жидкостей не имеют таких особенностей – чтобы какой-то один параметр менялся по-разному на разных порогах температуры.
Круговорот воды в природе
Вода образует водную оболочку нашей планеты – гидросферу.
Её делят на Мировой океан, континентальные поверхностные воды и ледники, а также подземные водоёмы. Переходы H2O из одних частей гидросферы в другие составляют сложный круговорот воды на Земле
Круговорот воды в природе — это непрерывное движение воды в гидросфере Земли. В процессе этого обмена водная масса меняет агрегатное состояние: из жидкой или твердой превращается в газообразную и обратно.
Рассмотрим на примере.
- С поверхности океанов, морей, рек и суши вода в виде пара поднимается вверх.
- Высоко над землей он охлаждается и образует множество водяных капелек и льдинок. Из них образуются облака.
- В виде осадков вода возвращается на Землю.
1.1 ОСОБЕННОСТИ И РАЗНОВИДНОСТИ
Тяжеловодными называют реакторы, в
которых замедлителем является тяжелая вода (D2O).
Они наиболее экономичны в отношении расхода ядерного топлива, что обусловлено
свойствами D2O как замедлителя: тяжелая вода
обладает наивысшим коэффициентом замедления по сравнению как с обычной водой,
так и с графитом. В этих реакторах требуется минимальная загрузка топлива для
выработки единицы мощности. Тяжелая вода практически не поглощает тепловые
нейтроны, поэтому тяжеловодные реакторы могут работать на природном уране с
достаточной свободой выбора состава топлива и конструкции активной зоны.
Благодаря хорошему балансу нейтронов KB в этих
реакторах высок по сравнению с KB реакторов на тепловых
нейтронах других типов.
Основной недостаток тяжеловодных реакторов—высокая стоимость
тяжелой воды. Однако это практически полностью компенсируется низкой стоимостью
топливной составляющей. Тем не менее, при конструировании и эксплуатации
тяжеловодных реакторов необходимо позаботиться о сведении к минимуму потерь D2O
Это тем более важно, что утечка тяжелой воды
определяет содержание паров трития в рабочих помещениях, токсичных и вредных
для организма человека
Пробег нейтронов в тяжеловодном замедлителе значительно
больше, чем в обычной воде (Н2О), поэтому решетка активной зоны
тяжеловодных реакторов делается редкой и габариты этих реакторов заметно
превышают размеры водо-водяных реакторов. По габаритам тяжеловодные реакторы
близки к графитовым, поэтому в них сравнительно низкое удельное энерговыделение
в активной зоне (примерно на порядок ниже, чем в водо-водяных реакторах с водой
под давлением).
В качестве теплоносителя в тяжеловодных реакторах наибольшее
применение получила тяжелая и обычная вода. При использовании в качестве теплоносителя
тяжелой воды реакторы могут быть как корпусными, так и канальными. Однако если
учесть, что основная утечка идет в контуре циркуляции теплоносителя,
целесообразно отделить замедлитель с его весьма редкой решеткой от
теплоносителя, а это в конечном итоге приводит к варианту канального типа. В
реакторах с легководным теплоносителем конструкция активной зоны определяется
однозначно—с разделением теплоносителя и замедлителя без допущения какого-либо
контакта между ними.
Тяжеловодные реакторы с водным теплоносителем (D2O или Н2О) могут быть как кипящие,
так и без кипения воды в активной зоне. Для этих реакторов характерно высокое
давление теплоносителя, что обусловлено его теплофизическими свойствами.
В качестве теплоносителя в тяжеловодных реакторах можно
использовать газ. В некоторых странах сооружены единичные экземпляры прототипов
энергетических тяжеловодных реакторов с газовым теплоносителем. Это реакторы
корпусного типа.