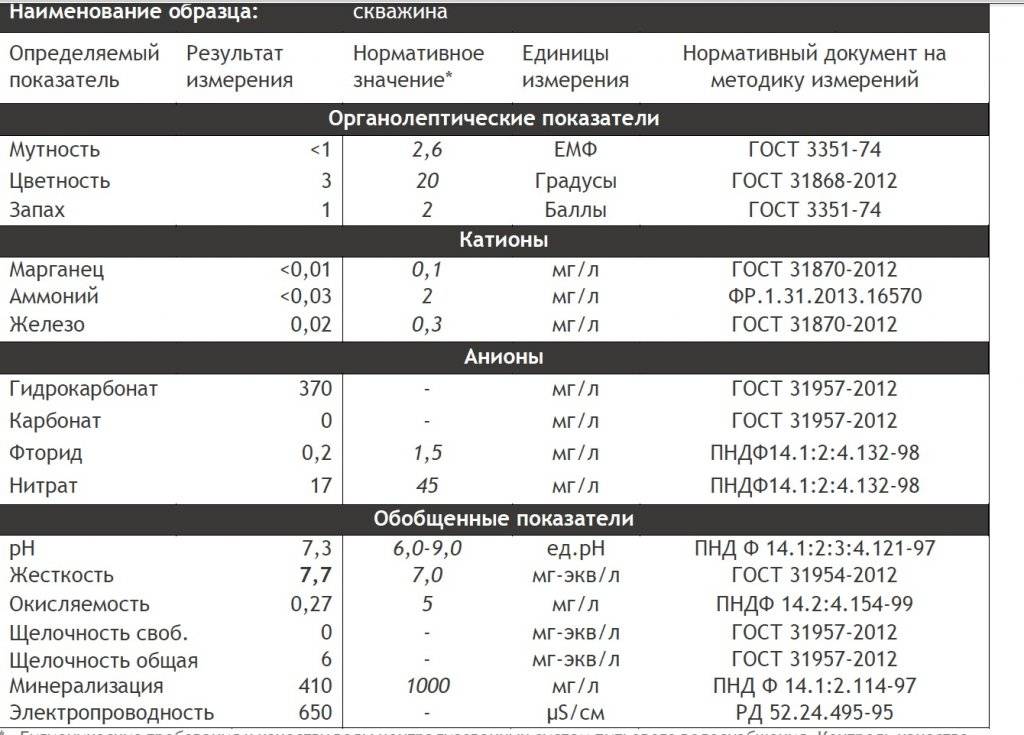
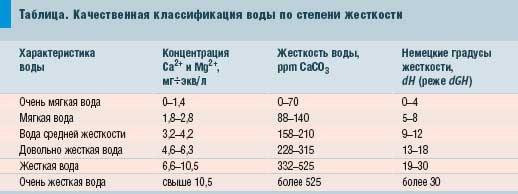
Способы изменения/коррекции pH
Ввиду нестабильности pH предпочтительно задавать направление реакции — в кислую или щелочную сторону. Быстрые изменения с помощью реагентов дают короткие результаты, через некоторое время водородный показатель вернётся на прежний уровень, характерный сложившейся биосистеме. Способ № 1. Поддержание pH возле отметки 7.0 и выше можно добиться использованием в оформлении известняка или мрамора, а также фильтра с мраморной крошкой в составе фильтрующего материала. Приводит к повышению жёсткости воды! Способ № 2. Добавление пищевой соды — обеспечивает быстрое отклонение водородного показателя в щелочную сторону, эффект достаточно продолжителен. Способ № 3. Уменьшение pH ниже отметки 7.0 обеспечивается установкой в аквариуме фильтра, где в качестве фильтрующего материала используется наполнитель на основе торфа. Способ № 4. Использование специальных реактивов pH+ и pH-. Порой не самый лучший выход из ситуации.
Мистер Хвост рекомендует: методы определения жесткости
Чтобы узнать значение водопроводной воды, пользуются несколькими способами.
При помощи TDS-метра
Компактный прибор, измеряющий концентрацию солей. Для проверки опустить устройство в жидкость и подождать, результат будет показан в миллиграммах на литр. Срок службы 1-2 года. Однако измерение можно считать относительным, так как, помимо кальция и магния, итоговое число будет содержать и незначительное количество примесей других веществ.
Полоски с нанесенными на них реагентами
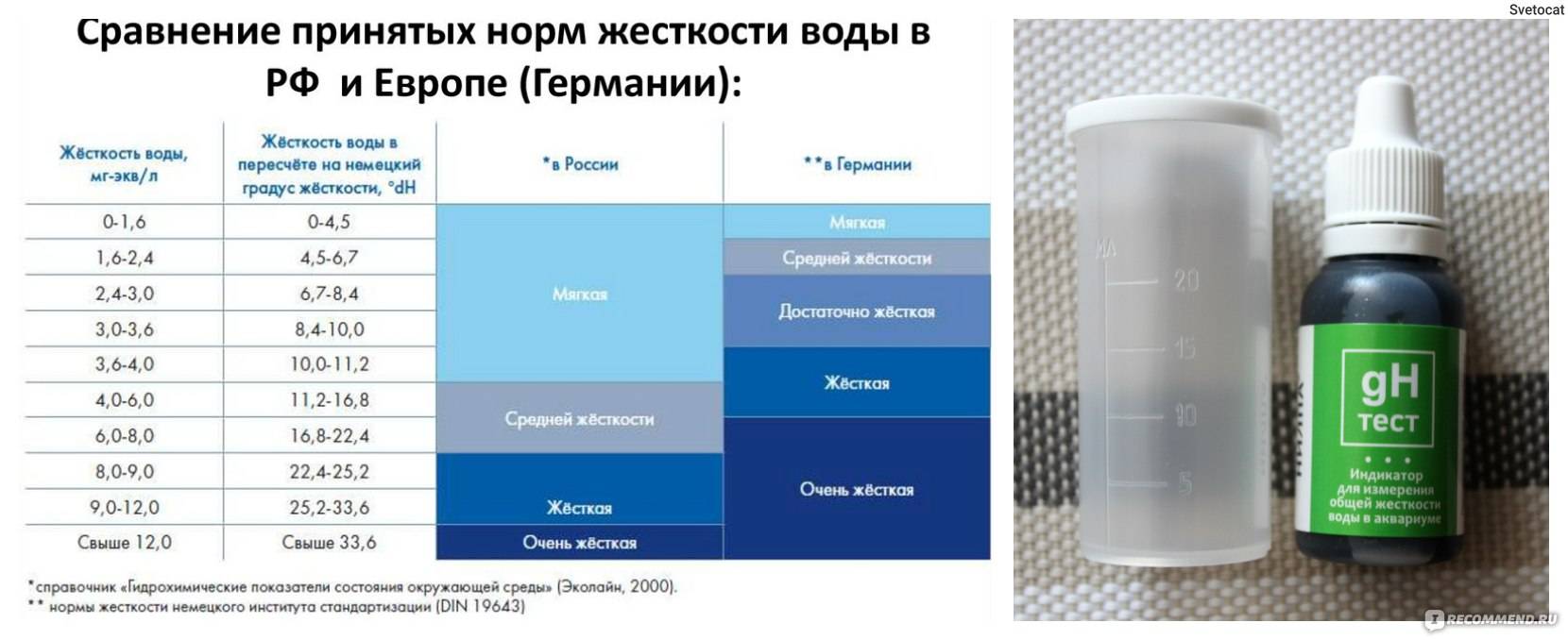
Их можно приобрести в магазине. Для определения жесткости нужно опустить лакмусовую бумажку в воду и дождаться изменения цвета. После соотнести полученный результат с предложенной в инструкции таблицей. Способ простой и доступный и может быть выполнен прямо в аквариуме. Но единицы измерения придется переводить из зарубежных в российские градусы.
Капельные тесты
Продаются в зоомагазинах. Для проверки: набрать 5 мл воды и добавить химический реактив из пузырька. Далее цвет жидкости изменится от красного до зеленого. После прохождения реакции количество капель реагента будет равно немецким градусам.
Химический реагент Трилон “Б”
Этот метод считается самым точным, минусами являются сложность и длительность проведения опыта. В воду, взятую из аквариума, добавляют буферную смесь, химический реагент и специальный индикатор. При прохождении реакции цвет раствора меняется от вишневого до сине-зеленого.
С помощью хозяйственного мыла
Считается самым доступным способом. Необходимы: 1 гр. измельченного мыла (60 или 72 %) и нагретая дистиллированная вода. Из них делается раствор и добавляется в банку, куда налито 0.5 л водопроводной воды. После появления шапки из пены — сигнала, что соли в жидкости связаны, — остаток мыльного раствора измеряется линейкой. Это значение отнимается от первоначального количества. Каждый сантиметр, полученный при вычитании, равен 2 градусам жесткости. Результат узнают из таблицы.
Среднее значение воды из крана равно 20 °, это высший допустимый предел для многих видов рыб.
Общие определения
Грязная и мутная жидкость портит общий вид, но кристально чистая также не всегда бывает полезной
После кислотности вторым по важности параметром является уровень жесткости. Его слишком высокие или низкие значения в первую очередь отразятся на растениях.
Жесткость разделяют на 3 вида:
- Общая (gH). Состоит двух значений приведенных ниже.
- Некарбонатная. Это постоянная величина уровня растворенных в жидкости хлоридов и сульфатов магния и кальция. Не изменяется при кипячении в домашних условиях. Однако может колебаться в течение 24 часов. Этому способствует наличие растений или время суток.
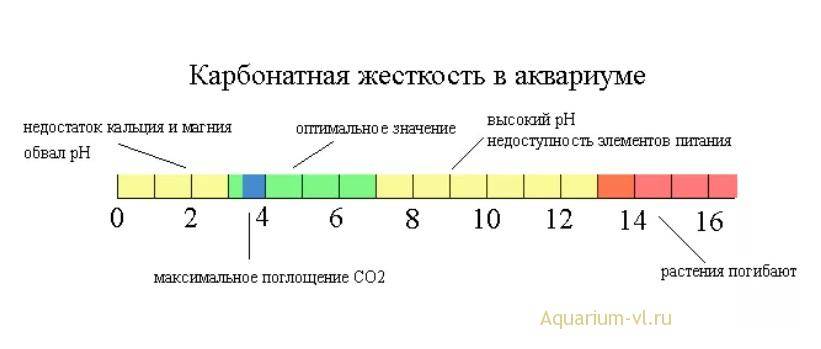
- Карбонатная (kH). Концентрация двууглекислых солей (Mg и Ca). При pH больше 8.3 и кипячении они образуют хлопьевидный осадок, оседают кристалликами на стенках емкости и пленку на поверхности воды.
Фото-галерея средств для измерения жесткости воды:
kH — наиболее важна для аквариумистов, это связано сразу с несколькими аспектами:
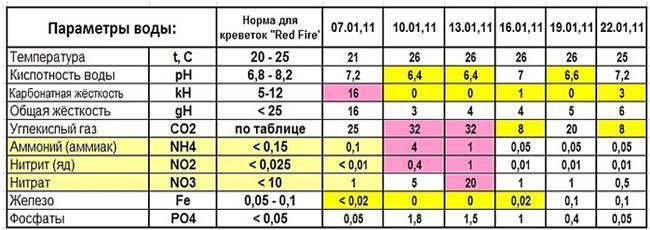
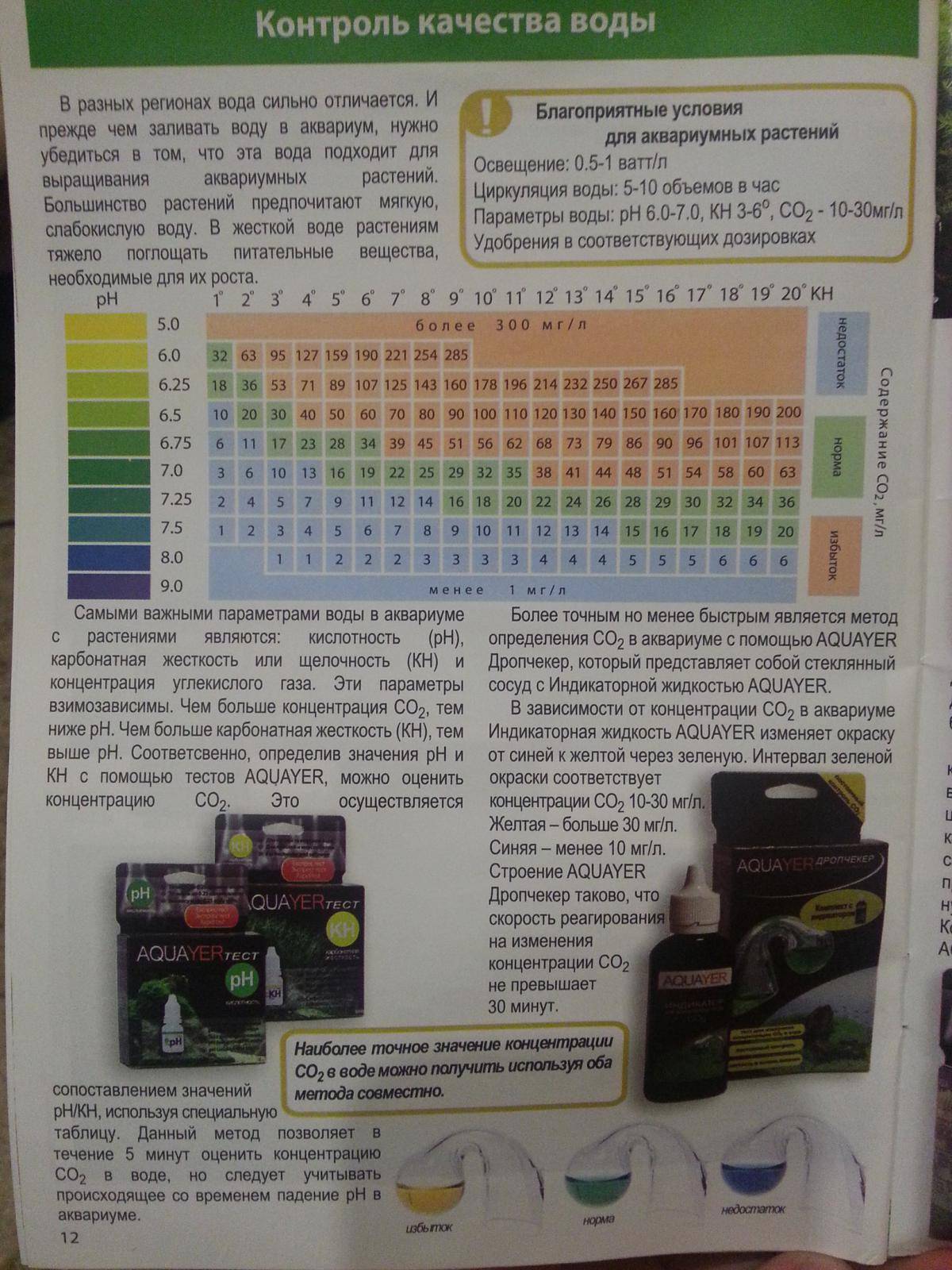
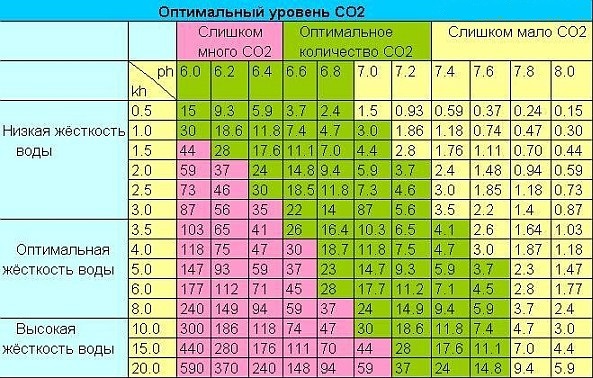
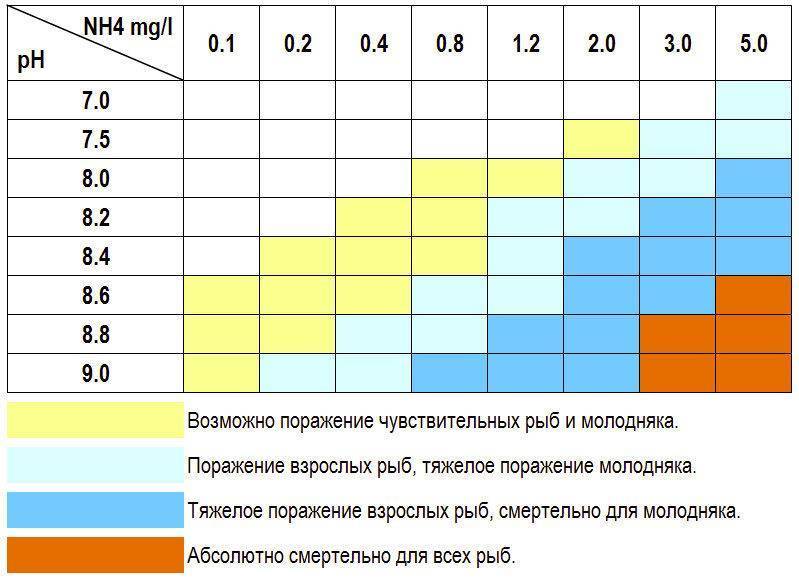
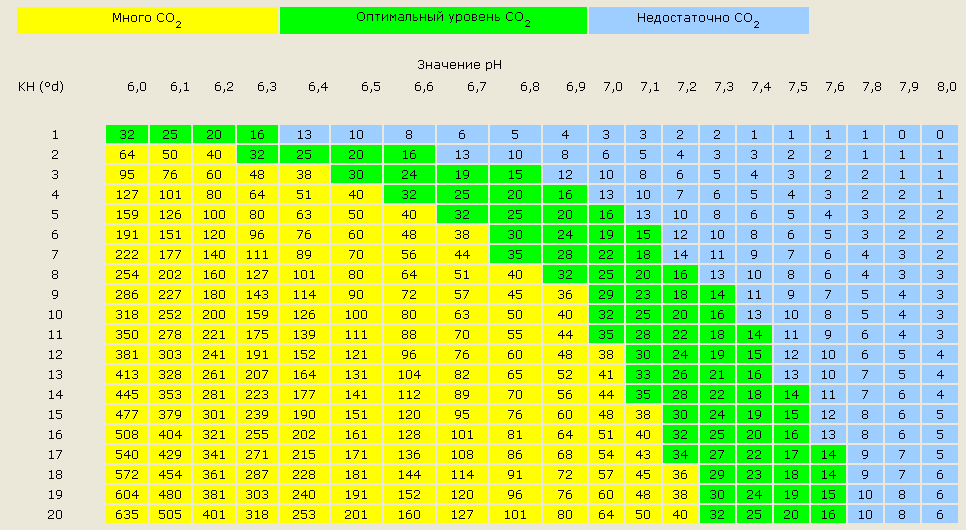
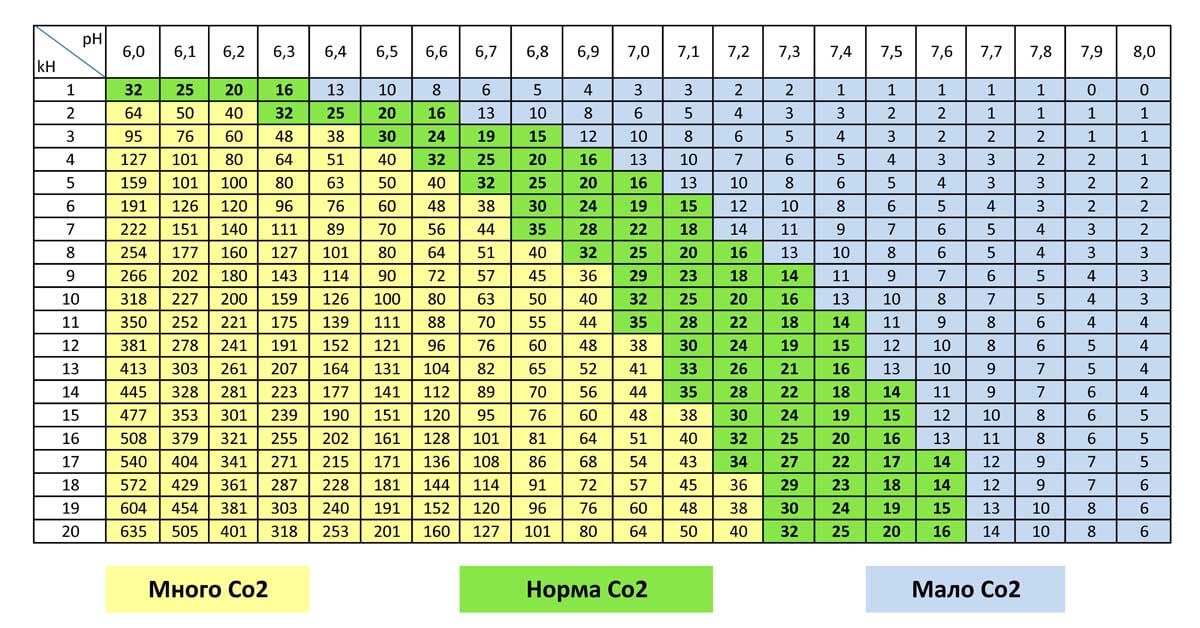
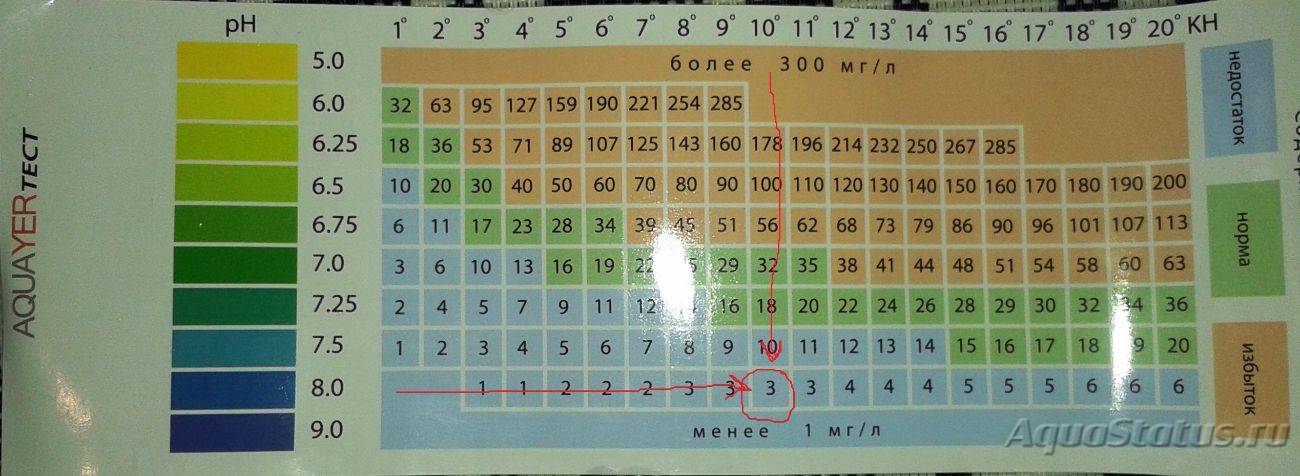
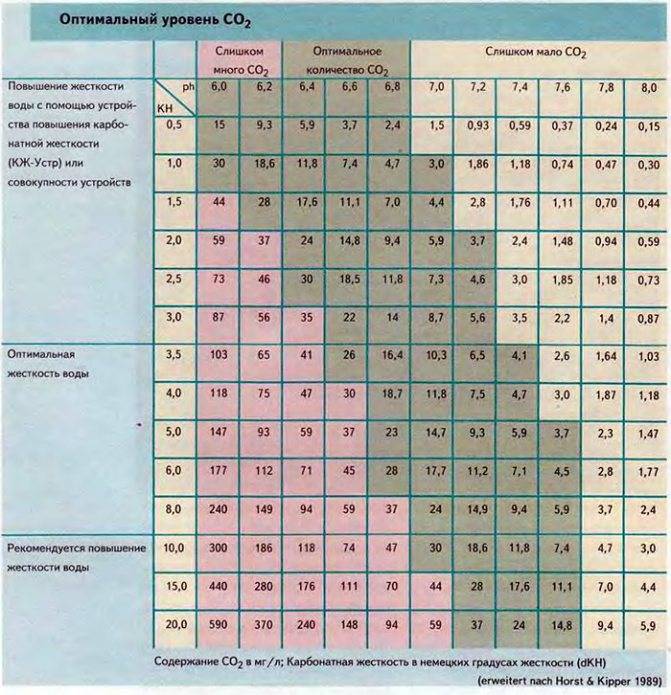
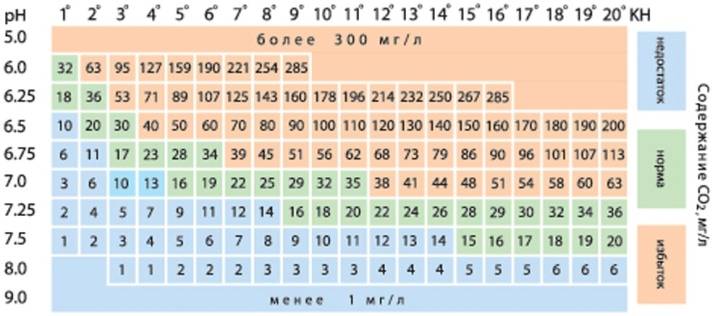
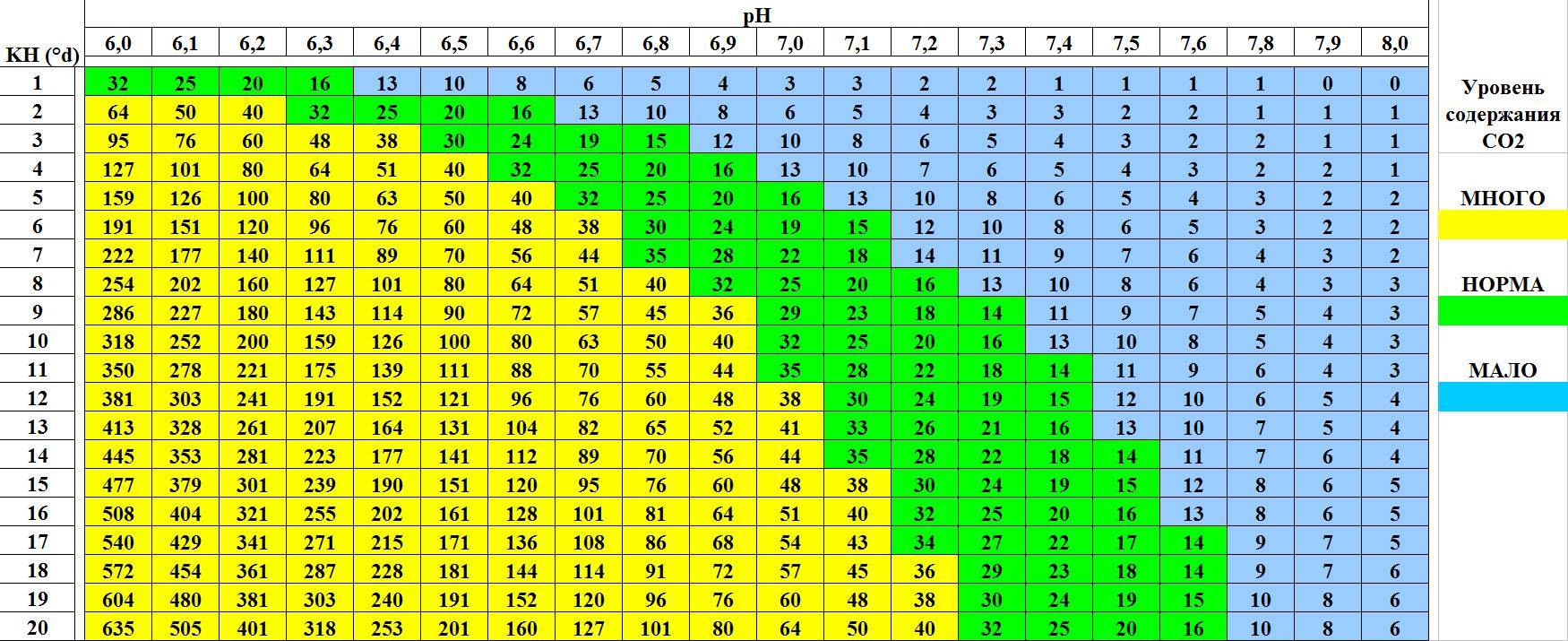
- Уровень углекислого газа, который образуется при дыхании рыбок. При высокой kH значение СО2 может достичь критической отметки свыше 30 мг/л, что приведет к гибели обитателей. Однако малая концентрация ниже 15 мг/л не позволит нормально развиваться растениям.
- Стабилизация pH. Между двумя значениями прямая зависимость.
- Вода для нереста некоторых видов рыб. Это жидкость с низкой kH и кислотностью в пределах 5.0-7.0.
Химические свойства воды
Химические свойства воды зависят от многих показателей и обусловлены ее свойством растворять различные вещества (она является универсальным растворителем), тем самым изменяя состав воды. Растворимость веществ в воде объясняется прежде всего тем, что в воде разноименные электрические заряды намного слабее притягиваются друг к другу чем в воздухе. При нагревании воды скорость растворения увеличивается. Вода как расворитель не изменяет растворенных веществ, т.е. является инертным растворителем, что имеет огромное значение для процессов жизнедеятельности, которые происходят с участием воды. Все необходимые питательные вещества доносятся водой в устойчивом виде. pH или активная реакция среды показывает количественное содержание ионов водорода (pH), определяющее реакцию, которая бывает нейтральной (pH=7), кислой (pH<7), щелочной (pH>7). Это очень важный показатель, который используется для определения различных свойств жидкости. Изменения pH воды меняют ее качества. Например, pH меньше 7 определяет реакцию воды как кислую, такая вода будет иметь кисловатый привкус; pH больше 10- реакция сильно щелочная, при которой вода становится особо мылкой, раздражает кожу и слизистые оболочки. В жидкостях организма поддерживается постоянный уровень pH, необходимый для нормальной жизнедеятельности (так, pH крови- 7,2-7,4; желудочного сока- 1,2-1,5 и т.п.). Окисляемость определяется по наличию растворенных органических веществ в воде и служит индикатором загрязненности. Показатель окисляемости чистой воды составляет 2-3 мг/л. Жесткость воды является одним из показателей ее качества. Она определяется по количеству содержащихся в ней солей кальция, магния (карбонатов, сульфатов и т.п.) и выражается в миллиграмм-эквиваленте на литр. Жесткость воды может быть постоянной и непостоянной. Постоянная жесткость обусловлена присутствием некарбонатных солей, растворимых в воде. Такая жесткость не устраняется при кипячении. Непостоянная (временная) или карбонатная отличается присутствием большого количества растворимых солей (карбонатов), которые становятся нерастворимыми при кипячении и выпадают в осадок (образуя накипь). Наибольшей мягкостью отличаются воды поверхностных источников воды, дождевая и талая воды. В подземных источниках жесткость воды зависит от глубины и места залегания, но в большинстве случаев она более высокая. Вязкость у воды незначительная, что обеспечивает ее текучесть и способность транспортировать различные вещества. При нагревании воды вязкость уменьшается. Соленая вода обладает большей вязкостью по сравнению с пресной. Изменять свойства воды можно различными способами- отстаиванием, замораживанием и размораживанием, кипячением, намагничиванием, добавлением различных химических веществ (минерализацией) и другими…
Все права защищены. При перепечатке материалов обязательно публиковать ссылку на сайт https://vodopoint.ru с указанием гиперссылки.
Что влияет на норму?
Выделяют следующие факторы, влияющие на содержание магния, кальция, карбонатов, меняющих состав:
Природа воды (водопроводная, дистиллированная, талая, родниковая, кипяченая).
- Состав водопроводной воды в определенной местности.
- Виды обитателей и продукты их метаболизма (рыбки, черепахи, водоросли).
- Период, за который не меняют воду, не очищают аквариум.
- Наличие или отсутствие фильтрации воды.
- Декор (гравий, крупные камни, замки).
- Наличие или отсутствие прямых солнечных лучей, падающих на растительность.
Даже если водопроводная вода в определенной местности обладает чрезмерными карбонатными показателями, их можно урегулировать
Это важно для аквариумов, где разводят дорогостоящие виды рыб
Газы в аквариумной воде
Баланс аквариума и здоровье рыбок зависит от наличия растворенных в воде газов. Дома определить количество газов невозможно. Можно просто наблюдать за поведением рыб, запахом исходящим из воды и делать соответствующие выводы.
Кислород
В аквариуме обязательно должен быть кислород. Им дышат рыбы, его потребляют растения. Без него не могут жить полезные бактерии, участвующие в процессах разложения органических соединений. В воду кислород поступает в процессе аэрации воды, а также фотосинтеза. На протяжении дня количество кислорода в воде изменяется. На его количество влияет температура воды. Чем она выше, тем меньше в ней содержится кислорода. В холодной воде кислорода больше, чем в теплой. Аэратор можно купить отдельно, но чаще всего он совмещен с внутренним фильтром.

Углекислый газ
Углекислый газ имеется в воде наравне с кислородом. Это продукт жизнедеятельности гидробионтов и растений (днем растения выделяют кислород, а ночью углекислый газ). Для хорошего роста растениям необходим углекислый газ, поэтому многие аквариумисты, содержащие травники, используют генераторы углекислого газа – система CO2. Дело в том, что от недостатка углекислого газа в воде растения медленно растут. Его количество меняется в течение дня и зависит от плотности посадки рыб и растений. Система CO2 стоит немалых денег, не каждому по карману, поэтому тщательнее выбирайте растения для своего аквариума. В её комплект входят: заправляемый газовый баллон, редуктор для регулирования давления, манометры для измерения давления газа до редуктора и после, электромагнитный клапан (вкупе с таймером открывает и закрывает баллон по расписанию), дроссель для тонкой настройки давления газа (количество пузырьков газа в минуту), трубки, счетчик пузырьков, тест количества углекислоты в воде, диффузор для эффективного растворения углекислоты в воде.
Сероводород
Имеет неприятный запах, появляется из-за гниения не съеденного рыбами корма и остатков гниющих листиков растений. Как правильно кормить рыбок, мы уже писали раньше. Выделение сероводорода происходит с поглощением кислорода. Из-за этого рыбам может начать не хватать кислорода.
Метан
Образование метана происходит при разложении погибших гидробионтов и отмерших растений. Он практически не растворяется в воде. Скапливается в заиленном грунте в виде небольших пузырьков. Появляется только в грязных аквариумах. Большое количество метана приводит к отравлению и гибели донных рыб.
Что влияет на норму?
Выделяют следующие факторы, влияющие на содержание магния, кальция, карбонатов, меняющих состав:
Природа воды (водопроводная, дистиллированная, талая, родниковая, кипяченая).
- Состав водопроводной воды в определенной местности.
- Виды обитателей и продукты их метаболизма (рыбки, черепахи, водоросли).
- Период, за который не меняют воду, не очищают аквариум.
- Наличие или отсутствие фильтрации воды.
- Декор (гравий, крупные камни, замки).
- Наличие или отсутствие прямых солнечных лучей, падающих на растительность.
Даже если водопроводная вода в определенной местности обладает чрезмерными карбонатными показателями, их можно урегулировать
Это важно для аквариумов, где разводят дорогостоящие виды рыб
Параметры, какая должна быть
Разные виды рыб выживают и размножаются в определенных условиях. Для одних оптимальна низкая жесткость, для других – средняя.
Но выделяют наиболее оптимальные параметры:
- 3-6 мг-экв/л карбонатной жесткости для недавно налитой воды.
- до 15 мг-экв/л, когда вода стоит долго.
На жизнедеятельность внутренней среды аквариума негативно влияет чрезмерно пониженная или повышенная жесткость. Это критические параметры.
| Вид критического параметра | Описание |
| Низкий | Происходит по причине недостатка или отсутствия кальция. Без него растительность существовать не может, так как прекращается ее рост. Поэтому минимальное значение составляет 4 мг-экв/л |
| Высокий | Приводит к выпадению осадка, постепенной гибели рыб. В такой среде затруднено дыхание, размножение, другие основные функции. Критичность появляется свыше 15 мг-экв/л |
Оптимальными считаются мягкие или средние показатели. Они колеблются при изменении внешних и внутренних факторов. Поэтому периодически делают замер тест-системой.
Нормальные показатели жесткости для аквариума
Уровень жёсткости значительно влияет на здоровье домашних питомцев. При неподходящих показателях рыбки и растительность могут не комфортно себя чувствовать, болеть или даже погибнуть, если не применять никаких действий.
На что влияет водная жесткость:
- соли, находящие в Ca и Mg, участвуют в построении рыбной костной системы,
- при хороших показателях жесткости, панцирь моллюсков становится прочным,
- создаёт комфорт аквариумным жителям и растительности, поэтому они хорошо развиваются и растут.
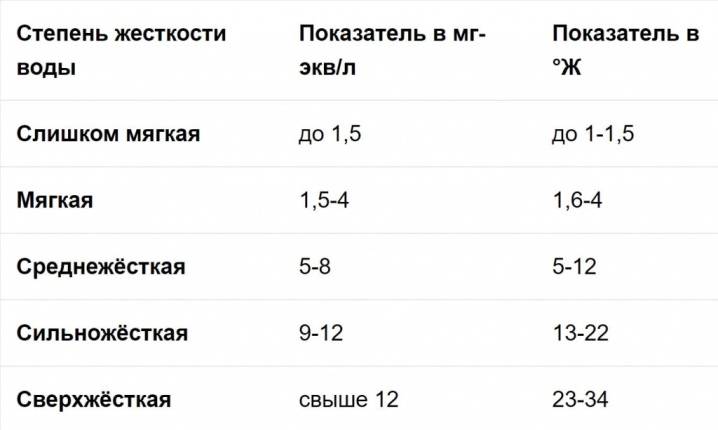
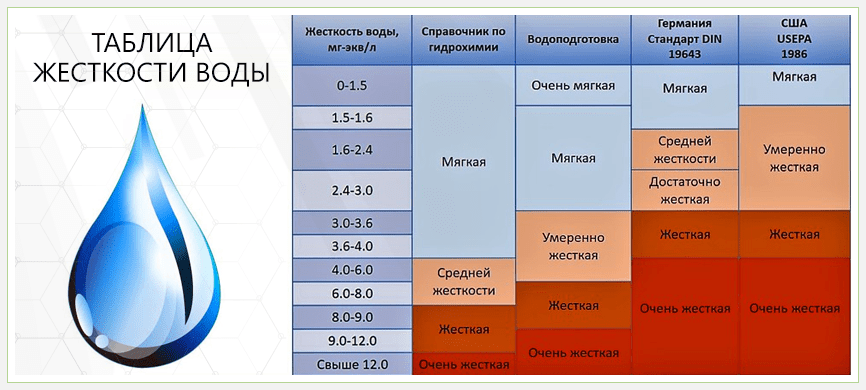
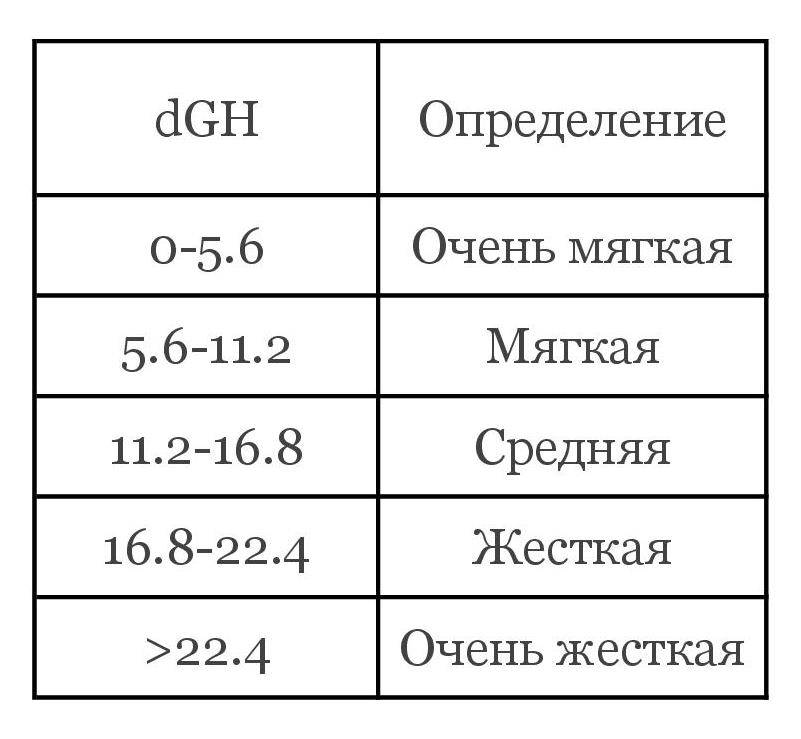
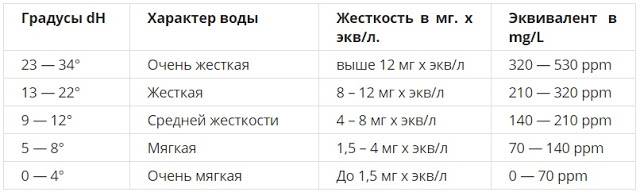
Интенсивность жёсткости:
- 0-4 – вода, обладающая слабой степенью интенсивности, очень мягкая,
- 5-8 – мягкая,
- 9-16 – жидкость, обладающая средней степенью жесткости,
- 17-32 – жесткая вода. К этому показателю приравнивается водопроводная жидкость,
- 33 и выше – повышенная степень жесткости.
Самый оптимальный вариант для разведения водных обитателей , максимально приближающийся показатель жесткости к водоёмной воде.
Например:
- для улиток нужна жесткая жидкость, чтобы обеспечить панцирную крепость,
- для неоновых рыбок хорошо использовать воду с уровнем – 6, а для живородящих рыб – 10,
- сагиттария, папоротник. Они проживают в температурных условиях 10-15℃. Более точную информацию о них можно узнать из источников по разведению конкретных видов рыб и растительности.
Посмотрите познавательное видео о жесткости воды:
Здесь рассказано почему может возникнуть необходимость снизить жесткость воды в аквариуме и как это сделать: приготовить воду нужной жесткости.
Понизить в аквариуме бывает необходимо, если хочется содержать мягководных рыб и выращивать растения, для которых оптимальной является мягкая слабокислая вода. При невысокой поддерживатьзначения рН в оптимальном для этих целей диапазоне: 6,4 – 6,7 будет относительно просто. Но в жесткой воде (при высоких значениях KH) сделать это .
Для того, чтобы приготовить нерестовую воду для мягководных рыб, также необходимо снизить ее жесткость. Уменьшить жесткость воды можно смешивая водопроводную жесткую воду с “осмосной”, дистиллятом, дождевой или талой. И тут возникает вопрос: а в какой пропорции смешивать, чтобы получить воду нужной жесткости? По сути дела, тут мы сталкиваемся с задачей разбавления раствора (воды из крана) до нужной концентрации. С вполне достаточной для аквариумных целей точностью она решается с помощью правила креста, или “конверта Пирсона”. Для этого нужно знать жесткость смешиваемых вод в градусах или их минерализацию, измеренную, например, кондуктометром. Определить жесткость можно с помощью капельных аквариумных тестов на общую жесткость и на карбонатную. Их точности будет вполне достаточно при приготовлении воды для мягководного аквариума.
При приготовлении нерестовой воды для таких требовательных видов, как красный неон (Paracheirodon axelrodi), желательно пользоваться кондуктометром, который позволяет получать более точные данные о степени минерализации воды.
Рассмотрим конкретный пример: карбонатная жесткость водопроводной воды – 10о KH, обессоленной с помощью недорогой системы обратного осмоса воды – 0,5о KH, требуется получить воду с карбонатной жесткостью – 2о KH. Графически правило креста можно представить так:
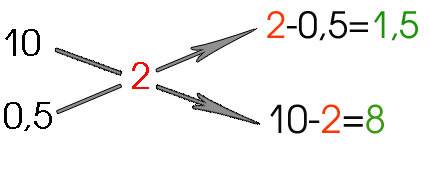 |
| Рис 1. Применение “конверта Пирсона”, или правила креста при приготовлении раствора заданной концентрации. В нашем случае это приготовление воды нужной жесткости. Сначала записывают одно над другим значения KH водопроводной и “осмосной” воды, справа между ними – нужное значение KH для воды, которую готовим. Далее крест-накрест вычитают из большего значения меньшее. Полученные разности показывают, сколько частей надо взять водопроводной и “осмосной” воды для смешивания. |
Все достаточно очевидно. Для того, чтобы получить воду с карбонатной жесткостью 2о KH надо смешать полторы части водопроводной воды с восемью частями “осмосной”.
Еще пример: здесь минерализация воды оценивается по ее проводимости в микроCименсах (μS). Поставлена цель приготовить очень мягкую, пригодную для нереста мягководных рыб воду с низкой проводимостью – всего лишь 30 μS. При этом проводимость водопроводной воды равна 600 μS, а осмосной – 10 μS.
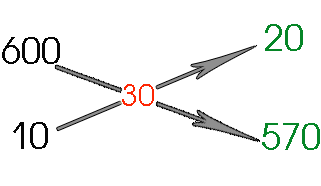 |
| Рис 2. Применение правила креста при приготовлении воды для аквариума заданной минерализации, выраженной в микроСименсах. |
Как следует из представленной схемы расчета, надо смешать 20 частей водопроводной воды с 570 частями “осмосной”. Для удобства использования результатов этого расчета, поделим их на 20, тогда получим пропорцию смешивания 1:28,5. То есть, для приготовления 29,5 л нерестовой воды нужно смешать 1 л водопроводной с 28,5 осмосной. Следует отметить, что приготовление нерестовой воды на этом не заканчивается. Но о нерестовой воде есть отдельная статья.

1) Не всегда водопроводная вода бывает жесткой, но в данной статье мы рассматриваем именно такой и наиболее часто встречающийся случай. Поэтому задача понижения жесткости водопроводной воды актуальна для многих аквариумистов..
2) Как общая, так и карбонатная жесткость измеряются в градусах. Аквариумиста обычно больше интересует карбонатная, так как она необходима для расчета содержания СО2 в воде аквариума, от нее и она же оказывает влияние на процесс оплодотворения икры и, следовательно, контроль карбонатной жесткости очень важен при приготовлении нерестовой воды. Карбонатная и общая жесткость обычно взаимосвязаны (если только в аквариум не добавляли соду), как правило карбонатная жесткость меньше общей на несколько градусов. Соли жесткости в пресных поверхностных водах вносят основной вклад в минерализацию воды. Поэтому чем ниже минерализация, тем ниже и жесткость..
3) Точность тестов для определения KH аквариумной воды (до одного градуса) вполне достаточна для решения большинства стоящих перед аквариумистом задач, но не для всех. Например, для разведения красного неона требуется минимальная карбонатная жесткость (менее 0,5о KH), поэтому для ее оценки лучше пользоваться кондуктометром..
Как определить уровень жесткости
Вода для её обитателей имеет такое же значение, как воздух для нас, поэтому она должна соответствовать условиям жизни обитателей аквариума. Рассмотрим, как можно определить жесткость воды в домашних условиях.
Знаете ли вы? Самый дорогой аквариум от компании Aquavista UK был разработан дизайнером Стюартом Хьюзом. Основной материал — золото высшей пробы, декор был выполнен из бивней мамонта и костей тираннозавра. Вес оригинальной ёмкости вместе с практической комплектацией (фильтры, терморегуляторы и прочее) составил 70 кг, а цена — 4 800 000 долларов.
Солемер (кондуктомер)
Солемер — прибор, который измеряет содержание соли в водной среде, приборы укомплектованы подробной инструкцией по применению с таблицами и значениями, по которым можно сделать интересующие расчёты.
Для домашнего пользования лучше всего подойдут ручные или портативные приборы. Первый оснащён стационарными или съёмными электродами, заключенными в водонепроницаемый корпус, благодаря умеренной цене пользуется особой популярностью.
Портативные устройства автоматизированы, имеют встроенную память, несколько функций, питаются либо от сети, либо от аккумуляторов.

Тест-полоски
Приобрести тест-полоски можно в точках продажи очистных фильтров. Это, по сути, лакмусовая бумажка, меняющая свой цвет при контакте с различными субстанциями.
В спецтестах для аквариумов присутствует таблица цветов и подробная инструкция по применению. Есть более дорогие наборы, укомплектованные дополнительно реактивами, обычно импортные.
Хозяйственное мыло
Самый простой и не требующий особых затрат метод — определить значение с помощью хозяйственного мыла. Он основан на свойстве мыла связывать соли. Для проведения процедуры понадобится дистиллированная вода, приобрести её можно в автомагазине.
Последовательность действий:
- В мерном стакане разведите измельчённый грамм мыла 72% в небольшой дозе воды.
- Долейте дистиллированную жидкость до уровня 7 см, каждый сантиметр равен 1° dH в 1 литре.
- В банку объёмом в литр наберите 500 мл воды, которую исследуете, добавляйте разведённый в мерном стакане раствор, помешивая до образования устойчивой пены (она будет означать, что соли связаны).
- Посмотрите, какое количество мыльного раствора пришлось потратить: каждый сантиметр равен 2° dH. Это значит, если затрачено 4 см мыльного раствора, жёсткость равна 8° dH.
- Отсутствие пены означает, что значение превышает 12° dH.
От редакции : Мох ключевой

Что это такое?

Жесткость воды – параметр, отображающий концентрацию солей, формирующихся благодаря щелочноземельным металлам. К ним относят магний, кальций, вспомогательные элементы. Чем больше веществ концентрируется в воде, тем выше ее жесткость. Это не означает, что параметр должен быть полностью исключен.
Нужен качественный баланс веществ для поддержания нормальной жизнедеятельности растений, рыб.
Общая
Общая жесткость – все количество солей кальция и магния, присутствующих в воде. Она делится на следующие виды:
- Карбонатная или временная.
- Некарбонатная – постоянная.
Общий параметр отражает все количество элементов, которые формируют щелочную среду. Он постоянно меняется, так как микроэлементы осаждаются, рыбы и растительность выделяют продукты метаболизма.
Карбонатная
Карбонатная жесткость указывает на наличие анионов гидрокарбоната, бикарбоната. Кислотно-основное состояние сильно повышается.

Выделяют следующие особенности:
- формирование осадочных частиц;
- в процессе кипячения осадочные вещества формируются в большей степени, дополнительно выделяется газ;
- ph меньше, чем у схожих показателей.
Некарбонатная
Некарбонатная жесткость не меняется под влиянием разных веществ и термической регуляции. Она появляется благодаря следующим свойствам:
- постоянно действующие соли;
- содержание Cl, SO4.
Вещества поддерживают среду на оптимальном уровне. Оба вида жесткости взаимодействуют. Но последний параметр есть всегда, вне зависимости от условий.
Как понизить?
Понизить жесткость немного сложнее. Нужно быть осторожным, в кислой среде погибает большинство видов рыб и растений.
Домашние рецепты
Применяют следующие народные методы, понижая количество солей:
Сделать смесь из водопроводной и дистиллированной водой.
- Кипячение. Водопроводную воду кипятят на огне 1 час. В аквариум добавляют только верхние слои, так как на дно соли выпадают в осадок.
- Замораживание. В емкость добавляют воду, которую отправляют в морозильную камеру. Дожидаются, когда она покроется толстой корочкой. В ней пробивают отверстие, выливая жидкое содержимое. Лед топят, наливая в аквариум.
Это самые простые способы, которые может применить любой человек. Не нужно покупать дополнительные ингредиенты.
Фильтры
Химические методы включают в себя систему фильтрации. Можно применить как разные вещества, так и электронные системы.
Применяют следующие виды фильтров:
- осмотический;
- деионизирующий;
- торфяной.
Первые 2 метода применяют с помощью готовой системы.
Если используют торфяной фильтр, воду предварительно кипятят. После фильтрации она приобретет желтый оттенок. Его убирают активированным углем.
Что это такое?
Жесткость воды – параметр, отображающий концентрацию солей, формирующихся благодаря щелочноземельным металлам. К ним относят магний, кальций, вспомогательные элементы. Чем больше веществ концентрируется в воде, тем выше ее жесткость. Это не означает, что параметр должен быть полностью исключен.
Нужен качественный баланс веществ для поддержания нормальной жизнедеятельности растений, рыб.
Общая
Общая жесткость – все количество солей кальция и магния, присутствующих в воде. Она делится на следующие виды:
- Карбонатная или временная.
- Некарбонатная – постоянная.
Общий параметр отражает все количество элементов, которые формируют щелочную среду. Он постоянно меняется, так как микроэлементы осаждаются, рыбы и растительность выделяют продукты метаболизма.
Карбонатная
Карбонатная жесткость указывает на наличие анионов гидрокарбоната, бикарбоната. Кислотно-основное состояние сильно повышается.
Выделяют следующие особенности:
- формирование осадочных частиц;
- в процессе кипячения осадочные вещества формируются в большей степени, дополнительно выделяется газ;
- ph меньше, чем у схожих показателей.
Некарбонатная
Некарбонатная жесткость не меняется под влиянием разных веществ и термической регуляции. Она появляется благодаря следующим свойствам:
- постоянно действующие соли;
- содержание Cl, SO4.
Вещества поддерживают среду на оптимальном уровне. Оба вида жесткости взаимодействуют. Но последний параметр есть всегда, вне зависимости от условий.