Литература
- Кипение // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Исаченко В. П., Осипова В. А., Сукомел А. С. Теплопередача. — М.: Энергия, 1969.
- Кикоин И. К., Кикоин А. К. Молекулярная физика. — М., 1963.
- Радченко И. В. Молекулярная физика. — М., 1965.
- Михеев М. А. Глава 5 // Основы теплопередачи. — 3-е изд. — М.—Л., 1956.
- Петухов Б. С., Генин Л. Г., Ковалев С. А. Теплообмен в ядерных энергетических реакторах. — М.: Энергоатомиздат, 1986.
- Кириллов П. Л., Юрьев Ю. С., Бобков В. П. Справочник по теплогидравлическим расчетам. — М.: Энергоатомиздат, 1990.
- Кипение // : / гл. ред. А. М. Прохоров. — 3-е изд. — М. : Советская энциклопедия, 1969—1978.
См. Кипячение воды при комнатной температуре
Хотя непрактично посещать космос, чтобы увидеть, как вода закипает, вы можете увидеть эффект, не выходя из дома или учебы. Все, что вам нужно, это шприц и вода. Вы можете получить шприц в любой аптеке (игла не требуется) или во многих лабораториях.
- Наберите в шприц небольшое количество воды. Вам просто нужно достаточно, чтобы увидеть это – не наполняйте шприц полностью.
- Положите палец на отверстие шприца, чтобы закрыть его. Если вы боитесь поранить палец, можно прикрыть отверстие куском пластика.
- Наблюдая за водой, как можно быстрее потяните шприц назад. Вы видели, как закипает вода?
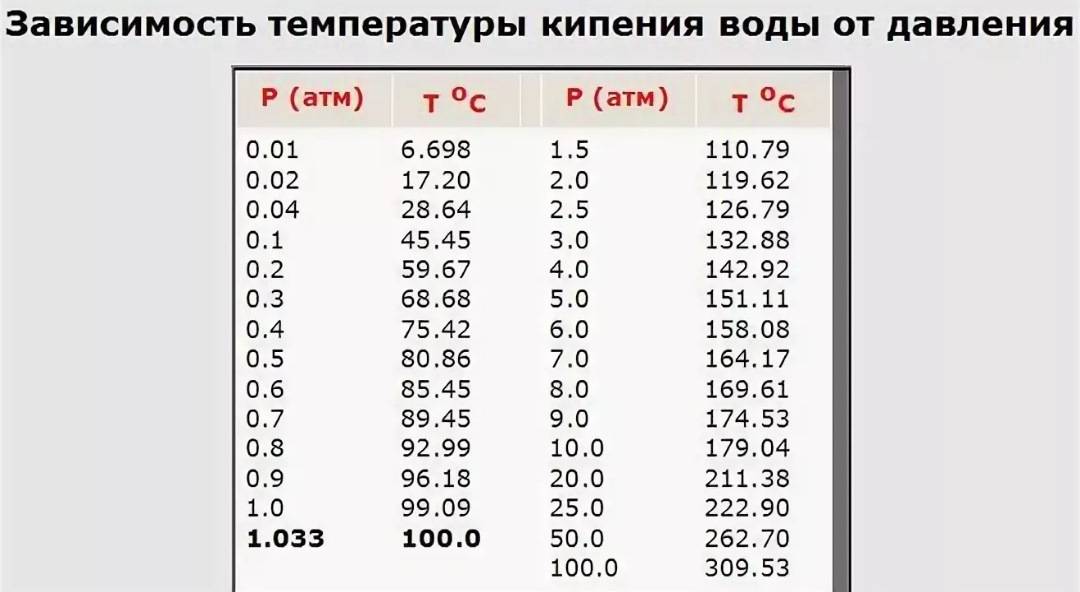
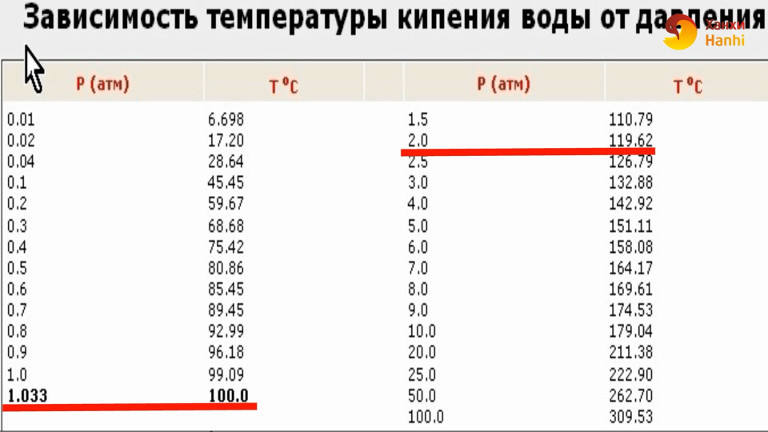
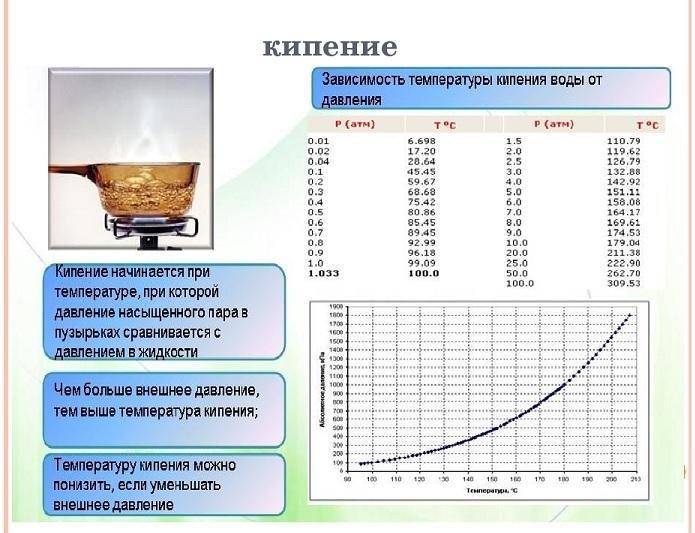
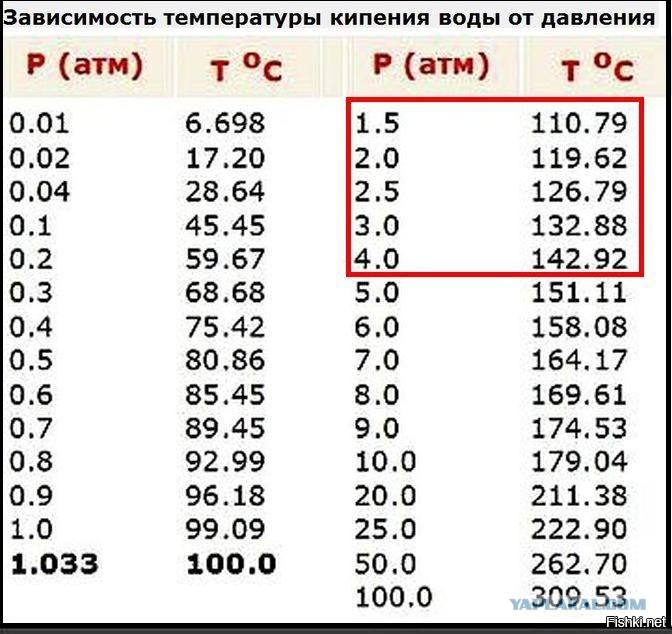
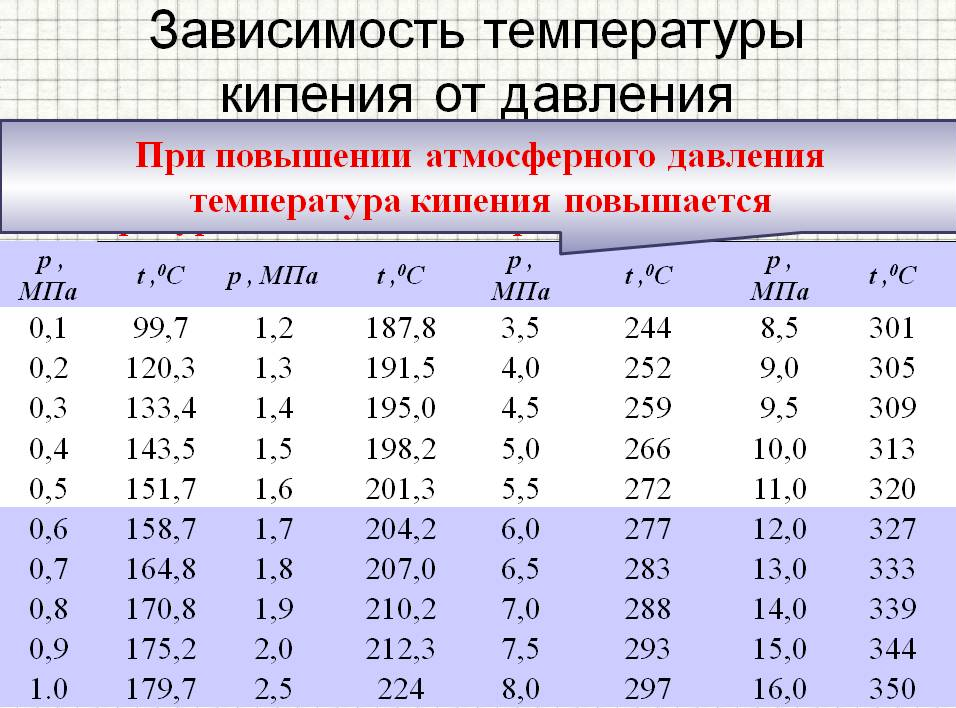
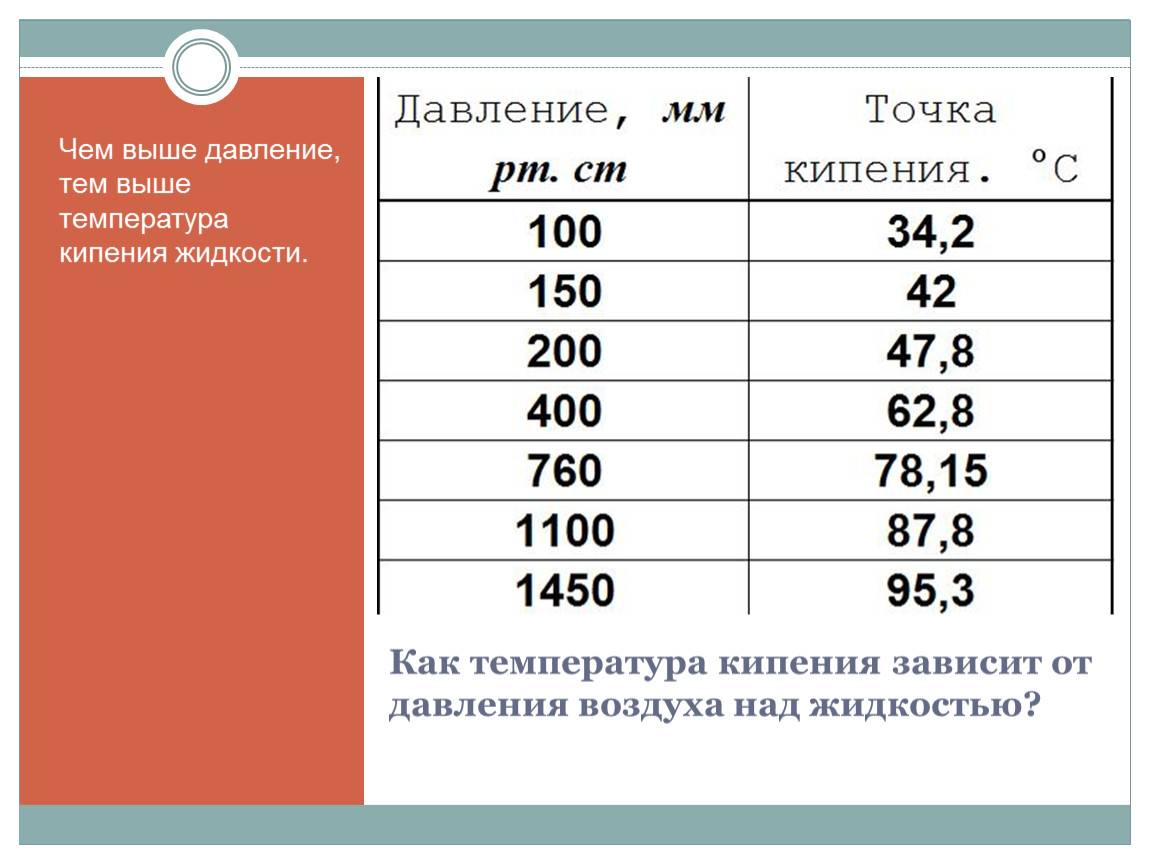
Зависимость температуры кипения жидкости от давления
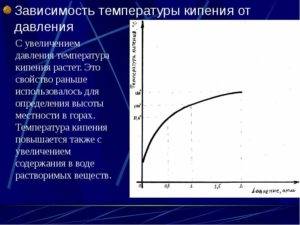
Из приведенныхрассуждений ясно, что температуракипения жидкости должна зависеть отвнешнего давления. Наблюдения подтверждаютэто.
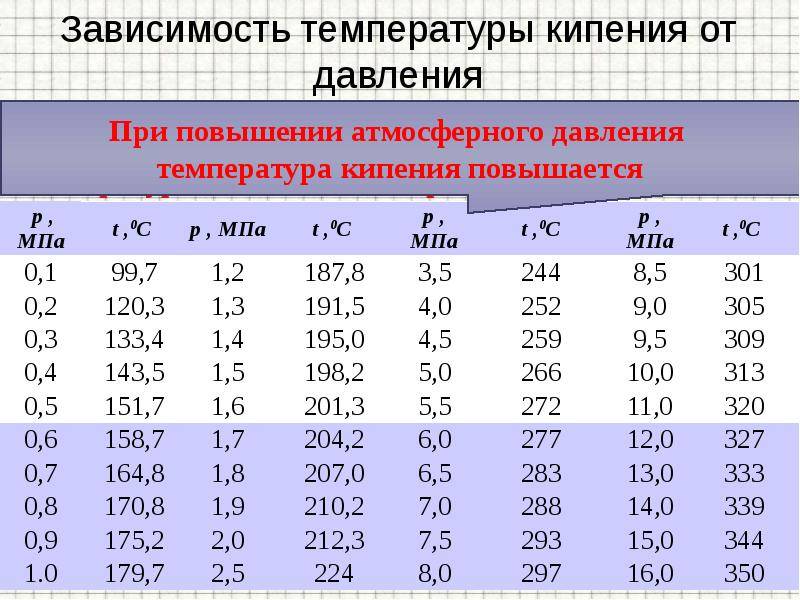
Чембольше внешнее давление, тем вышетемпература кипения. Так, в паровомкотле при давлении, достигающем 1,6 · 106Па, вода не кипит и при температуре 200°С.
В медицинских учреждениях кипениеводы в герметически закрытых сосудах— автоклавах (рис. 6.11) также происходитпри повышенном давлении. Поэтомутемпература кипения значительно выше100 °С.
Автоклавы применяют для стерилизациихирургических инструментов, перевязочногоматериала и т. д.
Рис. 6.11
Инаоборот, уменьшая внешнее давление,мы тем самым понижаем температурукипения. Под колоколом воздушного насосаможно заставить воду кипеть при комнатнойтемпературе (рис. 6.12).
При подъеме в горыатмосферное давление уменьшается,поэтому уменьшается температура кипения.На высоте 7134 м (пик Ленина на Памире)давление приближенно равно 4 · 104Па (300 мм рт. ст.). Вода кипит там примернопри 70 °С.
Сварить, например, мясо в этихусловиях невозможно.
Рис. 6.12
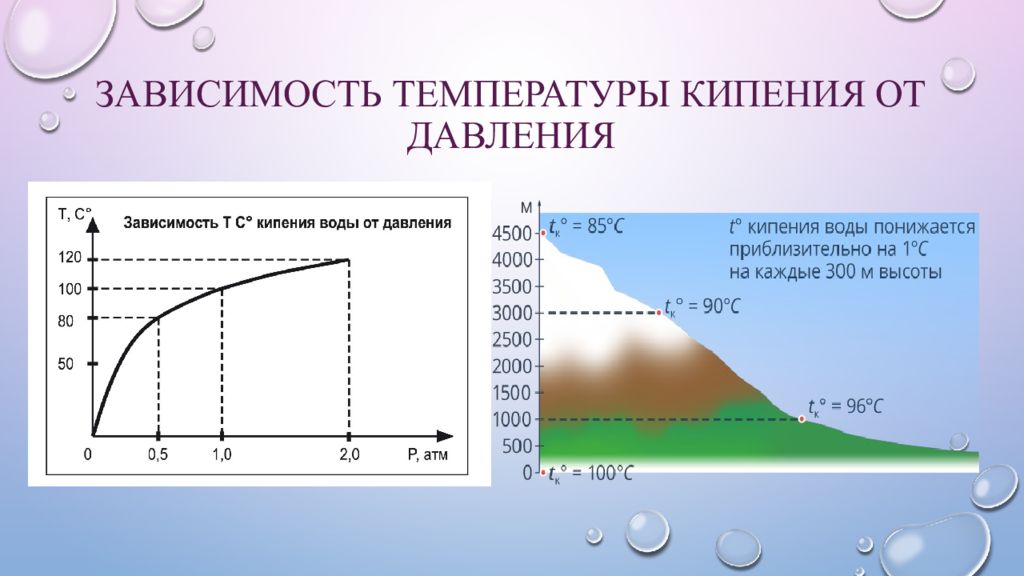
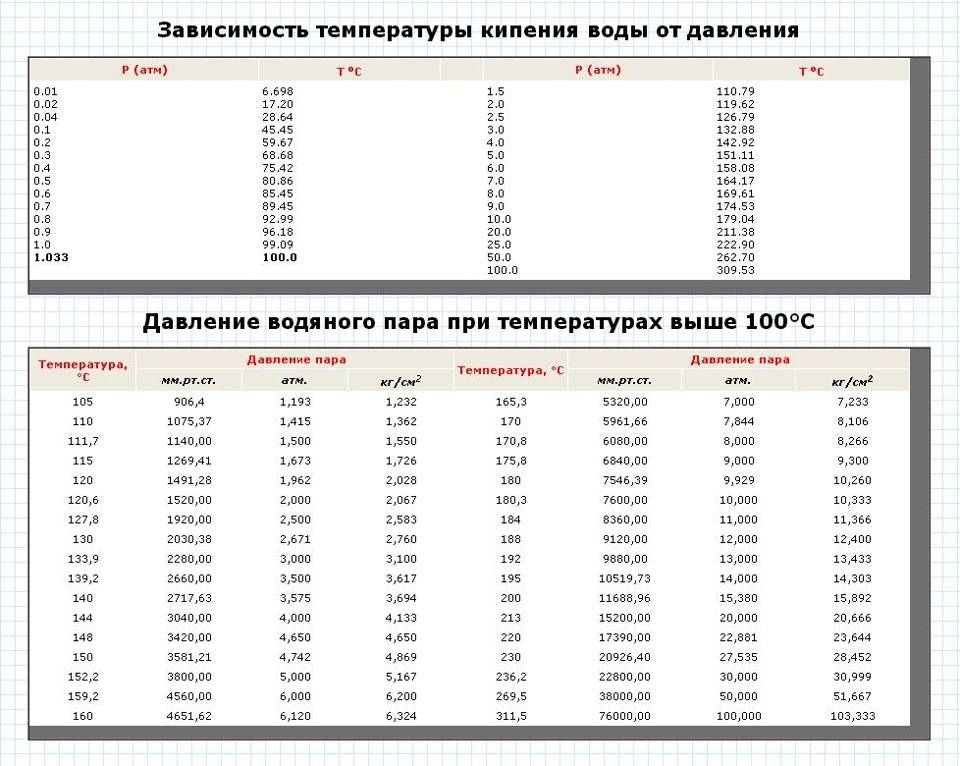
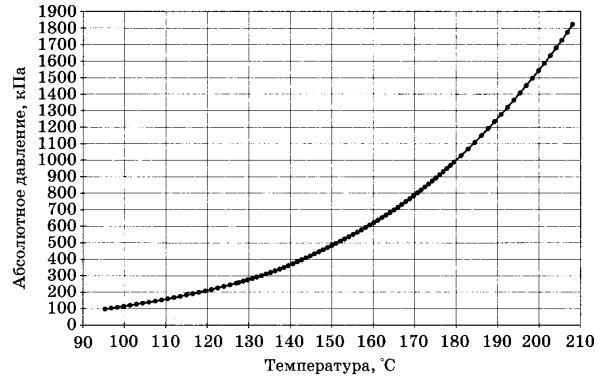
На рисунке 6.13изображена кривая зависимости температурыкипения воды от внешнего давления. Легкосообразить, что эта кривая являетсяодновременно и кривой, выражающейзависимость давления насыщенноговодяного пара от температуры.
Рис. 6.13
Различие температур кипения жидкостей
У каждой жидкостисвоя температура кипения. Различиетемператур кипения жидкостей определяетсяразличием в давлении их насыщенныхпаров при одной и той же температуре.Например, пары эфира уже при комнатнойтемпературе имеют давление, большееполовины атмосферного.
Поэтому, чтобыдавление паров эфира стало равныматмосферному, нужно небольшое повышениетемпературы (до 35 °С). У ртути же насыщенныепары имеют при комнатной температуресовсем ничтожное давление. Давлениепаров ртути делается равным атмосферномутолько при значительном повышениитемпературы (до 357 °С).
Именно при этойтемпературе, если внешнее давлениеравно 105 Па, и кипит ртуть.
Различие температуркипения веществ находит большоеприменение в технике, например приразделении нефтепродуктов. При нагреваниинефти раньше всего испаряются наиболееценные, летучие ее части (бензин), которыеможно таким образом отделить от «тяжелых»остатков (масел, мазута).
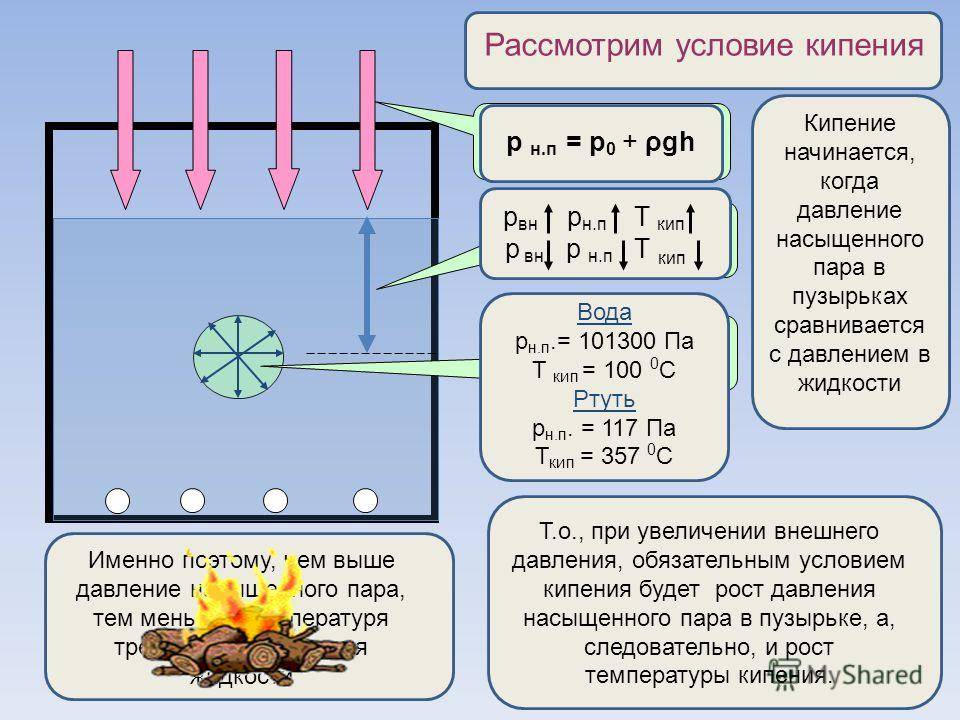
Жидкость закипает,когда давление ее насыщенного парасравнивается с давлением внутри жидкости.
§ 6.6. Теплота парообразования
Требуется лиэнергия для превращения жидкости в пар?Скорее всего да! Не так ли?
Мы отмечали (см. §6.1), что испарение жидкости сопровождаетсяее охлаждением. Для поддержаниятемпературы испаряющейся жидкостинеизменной к ней необходимо подводитьизвне теплоту.
Конечно, теплота и самаможет передаваться жидкости от окружающихтел. Так, вода в стакане испаряется, нотемпература воды, несколько болеенизкая, чем температура окружающеговоздуха, остается неизменной.
Теплотапередается от воздуха к воде до тех пор,пока вся вода не испарится.
Чтобы поддерживатькипение воды (или иной жидкости), к нейтоже нужно непрерывно подводить теплоту,например подогревать ее горелкой. Приэтом температура воды и сосуда неповышается, но каждую секунду образуетсяопределенное количество пара.
На что расходуетсяподводимая к телу энергия? Прежде всегона увеличение его внутренней энергиипри переходе из жидкого состояния вгазообразное: ведь при этом увеличиваетсяобъем вещества от объема жидкости дообъема насыщенного пара. Следовательно,увеличивается среднее расстояние междумолекулами, а значит, и их потенциальнаяэнергия.
Кроме того, приувеличении объема вещества совершаетсяработа против сил внешнего давления.Эта часть теплоты парообразования прикомнатной температуре составляет обычнонесколько процентов всей теплотыпарообразования.
Теплотапарообразования зависит от рода жидкости,ее массы и температуры. Зависимостьтеплоты парообразования от рода жидкостихарактеризуется величиной, называемойудельнойтеплотой парообразования.
Удельной теплотойпарообразования данной жидкостиназывается отношение теплотыпарообразования жидкости к ее массе:
(6.6.1)
гдеr— удельная теплота парообразованияжидкости; т—масса жидкости; Qn— ее теплота парообразования. Единицейудельной теплоты парообразования в СИявляется джоульна килограмм (Дж/кг).
Удельнаятеплота парообразования воды оченьвелика: 2,256·106Дж/кг при температуре 100 °С. У другихжидкостей (спирт, эфир, ртуть, керосини др.) удельная теплота парообразованияменьше в 3—10 раз.
Температура закипания воды
Существует два основных типа кипения воды: первоначальное, когда образуются небольшие пузырьки пара в отдельных точках, и критический тепловой поток, где кипящая поверхность нагревается выше некоторой критической температуры, и на поверхности образуется пленка пара. Переходное кипение является промежуточной, неустойчивой формой с элементами обоих типов.
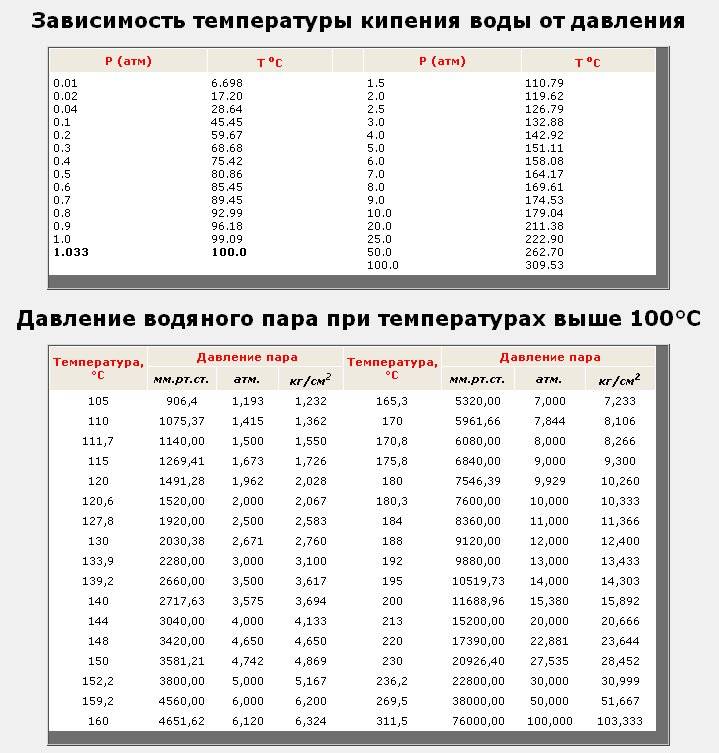
Температура кипящей воды обычно считается равной 100° C или 212° F при давлении 1 атмосферы (уровень моря). Однако, это значение не является константой. Многое зависит от атмосферного давления, которое изменяется в зависимости от высоты. Также на точку вскипания влияют такой фактор, как изменение состава воды.
Например, в городе Денвере, штат Колорадо, США, который находится на высоте около одной мили над уровнем моря, вода кипит приблизительно при 95° C или 203° F. Аналогичным образом, увеличение давления, как в скороварке, повышает температуру содержимого выше точки вскипания под открытым небом.
Добавление водорастворимого вещества, такого как соль или сахар также увеличивает градус закипания. При приемлемых концентрациях эффект очень мал и отличие трудно заметить. Однако, добавив достаточное количество соли или сахара, можно заметить повышение температуры кипячения. Из-за изменений в составе и давлении точка кипения почти никогда не составляет точно 100° C.
§ 34. Кипение. Зависимость температуры кипения от давления [1975 Ковалев П.Г., Хлиян М.Д. – Физика (молекулярная физика, электродинамика)]
Новости Библиотека Энциклопедия Биографии Ссылки Карта сайта О сайте
Парообразование может происходить не только в результате испарения, но и при кипении. Рассмотрим кипение с энергетической точки зрения.
В жидкости всегда растворено некоторое количество воздуха. При нагревании жидкости количество растворенного в ней газа уменьшается, вследствие чего часть его выделяется в виде маленьких пузырьков на дне и стенках сосуда и на взвешенных в жидкости нерастворенных твердых частичках.
Происходит испарение жидкости во внутрь этих воздушных пузырьков. Со временем пары в них становятся насыщенными. При дальнейшем нагревании увеличиваются давление насыщенного пара внутри пузырьков и их объем.
Когда давление пара внутри пузырьков становится равным атмосферному, они под действием выталкивающей силы Архимеда поднимаются на поверхность жидкости, лопаются, и из них выходит пар.
Парообразование, происходящее одновременно и с поверхности жидкости и внутри самой жидкости в воздушные пузырьки, называется кипением. Температура, при которой давление насыщенных паров в пузырьках становится равно внешнему давлению, называется температурой кипения.
Так как при одинаковых температурах давления насыщенных паров разнообразных жидкостей разные, то при различных температурах они становятся равными атмосферному давлению.
Это приводит к тому, что разные жидкости кипят при различных температурах. Данное свойство жидкостей используется при возгонке нефтепродуктов.
При нагревании нефти первыми испаряются наиболее ценные, летучие ее части (бензин), которые таким образом отделяются от “тяжелых” остатков (масел, мазута).
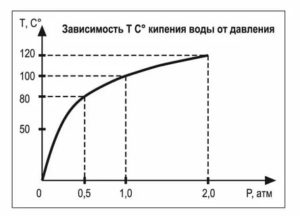
Рис. 37. Зависимость температуры кипения жидкости от давления
Из того, что кипение наступает, когда давление насыщенных паров равно внешнему давлению на жидкость, следует, что температура кипения жидкости зависит от внешнего давления. Если оно увеличено, то жидкость кипит при более высокой температуре, так как для достижения такого давления насыщенным парам необходима более высокая температура.
Наоборот, при пониженном давлении жидкость кипит при более низкой температуре. В этом можно убедиться на опыте. Нагреем воду в колбе до кипения и уберем спиртовку (рис. 37, а). Кипение воды прекращается.
При давлении 1 атм вода кипит при 100° С, а при 10 атм – при 180° С. Эта зависимость используется, например в автоклавах, в медицине для стерилизации, в кулинарии для ускорения варки пищевых продуктов.
Чтобы жидкость начала кипеть, ее следует нагреть до температуры кипения. Для этого надо жидкости сообщить энергию, например количество теплоты Q = cm(t°к – t°0). При кипении температура жидкости остается постоянной.
Так происходит потому, что сообщаемое при кипении количество теплоты затрачивается не на увеличение кинетической энергии молекул жидкости, а на работу разрыва молекулярных связей, т. е. на парообразование. При конденсации пар по закону сохранения энергии отдает в окружающую среду такое количество теплоты, которое было затрачено на парообразование.
Конденсация происходит при температуре кипения, которая в процессе конденсации остается постоянной. (Объясните почему).
Составим уравнение теплового баланса при парообразовании и конденсации. Пар, взятый при температуре кипения жидкости, по трубке А. поступает в воду, находящуюся в калориметре (рис.
38, а), конденсируется в ней, отдавая ей затраченное на его получение количество теплоты. Вода и калориметр получают при этом количество теплоты не только от конденсации пара, но и от жидкости, которая при этом получается из него.
Данные физических величин приведены в табл. 3.
Таблица 3
Конденсирующийся пар отдал количество теплоты Qп = rm3 (рис. 38, б). Жидкость, полученная из пара, охладившись от t°3 до θ°, отдала количество теплоты Q3 = c2m3 (t3° – θ°).
Рис. 38. К выводу уравнения теплового баланса при кипении и конденсации
Q1 = c1m1(θ° – t°2); Q2 = c2m2(θ° – t°2).
На основании закона сохранения и превращения энергии
Qп + Q3 = Q1 + Q2,
или
rm3 + c2m3 (t°2 – θ°) = c1m1(θ° – t°2) + c2m2(θ° – t°2).
Это уравнение называется уравнением теплового баланса при парообразовании и конденсации.
Задача 14. Перед тем как подать бревно в лесопильную раму, его в зимнее время освобождают от снега и льда, для чего оно некоторое время находится в бассейне, вода которого подогревается паром.
Рассчитать, какое количество 100-градусного пара расходуется за смену для плавления 5 т снега и льда и нагревания воды, полученной из них. Температура воздуха -20° С; конечная температура воды в бассейне стала 30° С.
Масса воды в бассейне 10 т, при работе бассейна ее температура повышается на 5° С.
Рис. 39. К задаче 14
По закону сохранения энергии:
Отсюда
Вычислим
Отв.: m1 ≈ 900 кг.
Как будет меняться температура кипения воды: 4 фактора
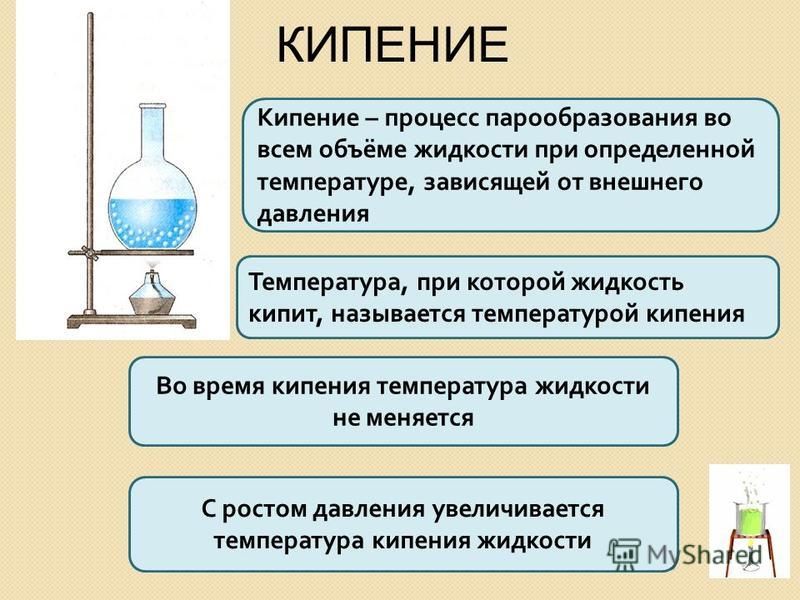
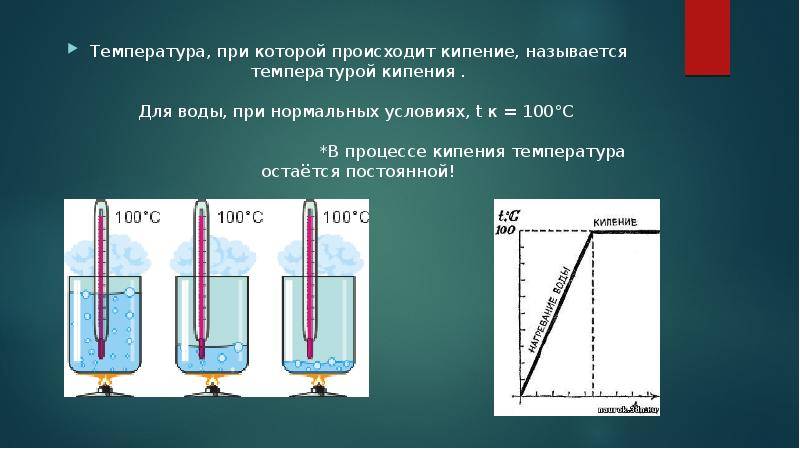
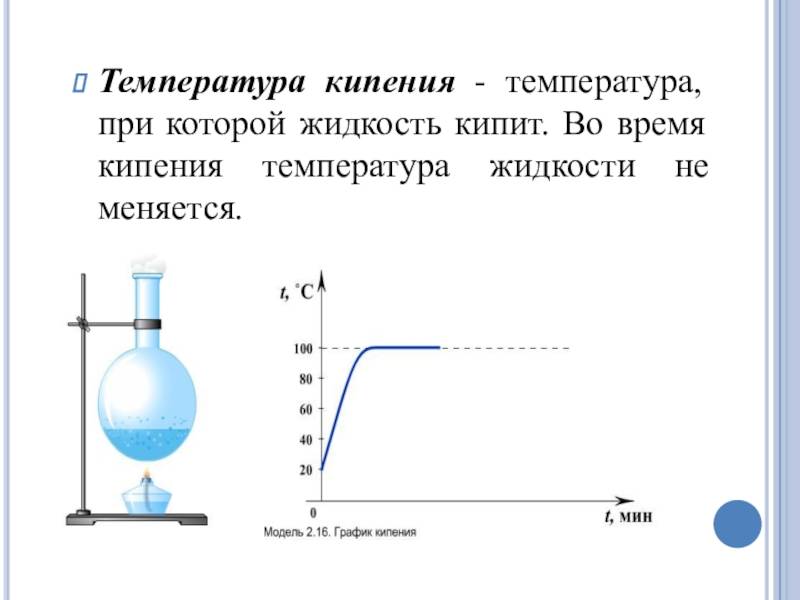
Температура, при которой кипит жидкость, называется температурой кипения.

Стоит отметить, что она всегда остается неизменной. Поэтому, если увеличить огонь под кипящей кастрюлей с водой, выкипать будет быстрее, но температура при этом не увеличится, так как средняя кинетическая энергия молекул остаётся неизменной.
Рассмотрим 4 фактора, которые влияют на изменение t°:
- Пониженное атмосферное давление (наблюдается в горной местности) – t° уменьшается.
- Повышенное атмосферное давление (наблюдается в шахте) – t° наоборот увеличивается.
- Применения герметической крышки, вакуума. За счёт герметической крышки или посуды пар не выходит градус кипения увеличивается. При использовании вакуума температура зависит от давления, которое создано внутри его.
- Свойства воды. Соленая вода начинает кипеть при более высокой температуре, чем пресная.
Рассмотрим более подробно каждый из факторов.
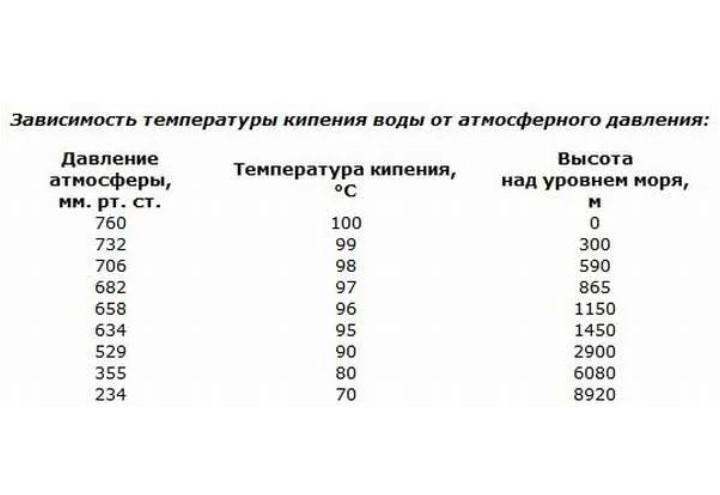
Влияние атмосферного давления
Согласно исследованиям и уравнению Клапейрона — Клаузиуса, градус кипения напрямую зависит от атмосферного давления. С его ростом температура кипения увеличивается, а с уменьшением, наоборот, становится все ниже и ниже.
Атмосферное давление — это давление атмосферы, действующее на все находящиеся на ней предметы и земную поверхность. Оно может меняться в зависимости от места и времени и измеряется барометром.
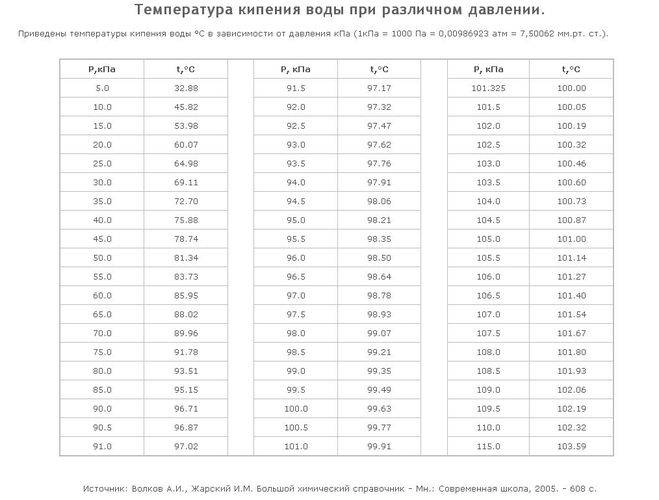
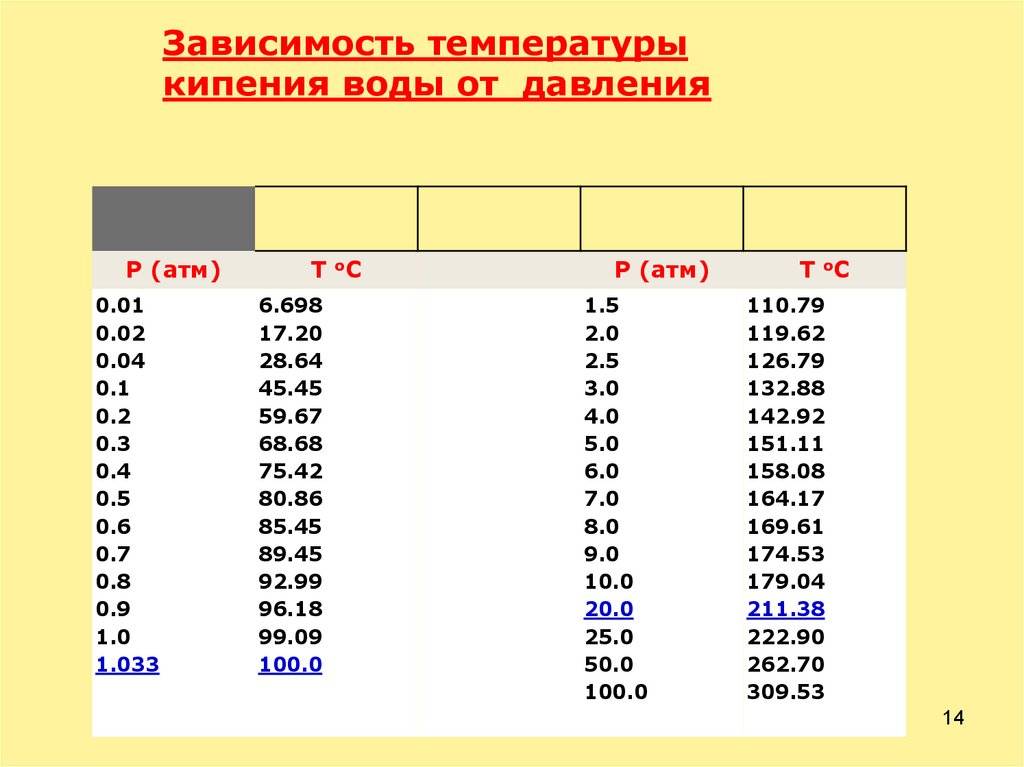
Таблица № 1. «Температура кипения воды от давления».
| Р, кПа | t, °C | Р, кПа | t, °C | Р, кПа | t, °C |
| 5,0 | 32,88 | 91,5 | 97,17 | 101,325 | 100,00 |
| 10,0 | 45,82 | 92,0 | 97,32 | 101,5 | 100,05 |
| 15,0 | 53,98 | 92,5 | 97,47 | 102,0 | 100,19 |
| 20,0 | 60,07 | 93,0 | 97,62 | 102,5 | 100,32 |
| 25,0 | 64,98 | 93,5 | 97,76 | 103,0 | 100,46 |
| 30,0 | 69,11 | 94,0 | 97,91 | 103,5 | 100,60 |
| 35,0 | 72,70 | 94,5 | 98,06 | 104,0 | 100,73 |
| 40,0 | 75,88 | 95,0 | 98,21 | 104,5 | 100,87 |
| 45,0 | 78,74 | 95,5 | 98,35 | 105,0 | 101,00 |
| 50,0 | 81,34 | 96,0 | 98,50 | 105,5 | 101,14 |
| 55,0 | 83,73 | 96,5 | 98,64 | 106,0 | 101,27 |
| 60,0 | 85,95 | 97,0 | 98,78 | 106,5 | 101,40 |
| 65,0 | 88,02 | 97,5 | 98,93 | 107,0 | 101,54 |
| 70,0 | 89,96 | 98,0 | 99,07 | 107,5 | 101,67 |
| 75,0 | 91,78 | 98,5 | 99,21 | 108,0 | 101,80 |
| 80,0 | 93,51 | 99,0 | 99,35 | 108,5 | 101,93 |
| 85,0 | 95, 15 | 99,5 | 99,49 | 109,0 | 102,06 |
| 90,0 | 96,71 | 100,0 | 99,63 | 109,5 | 102,19 |
| 90,5 | 96,87 | 100,5 | 99,77 | 110,0 | 102,32 |
| 91,0 | 97, 02 | 101,0 | 99,91 | 115,0 | 103,59 |
Единицы измерения давления в таблице: кПа.
Нормальное атмосферное давление составляет 765 мм. РТ. Ст. = 101,325 Р, кПа
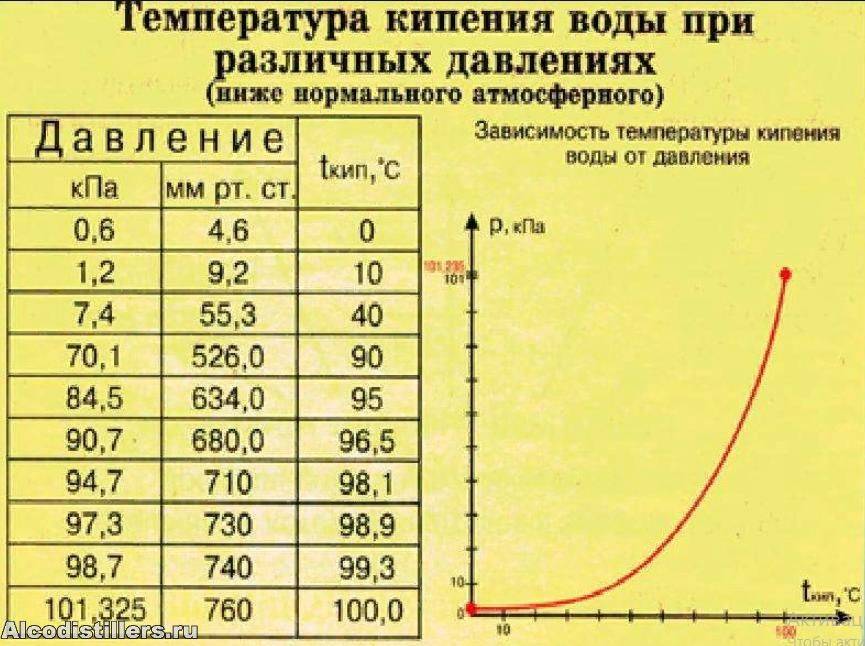
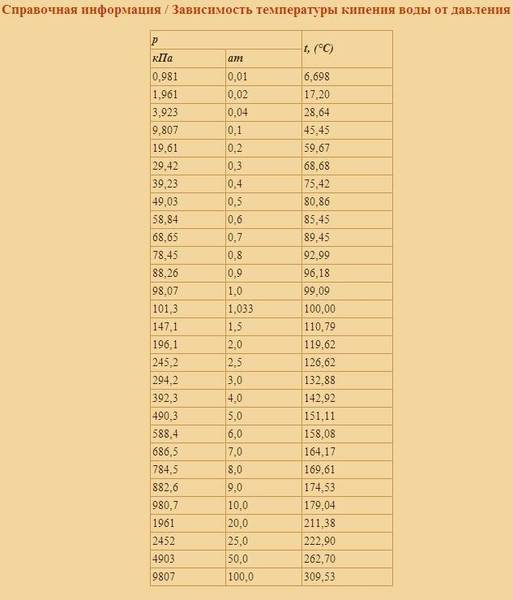
Температура кипения в горах
При подъеме над поверхностью Земли (в горах), температура кипения воды падает, так как снижается атмосферное давление (на каждые 10, 5 м на 1 мм РТ. С). Пузырькам легче всплывать – процесс происходит быстрее.

Для варки мяса, как и других продуктов, нужны привычные 100 градусов. В обратном случае все компоненты бульона просто останутся сырыми.
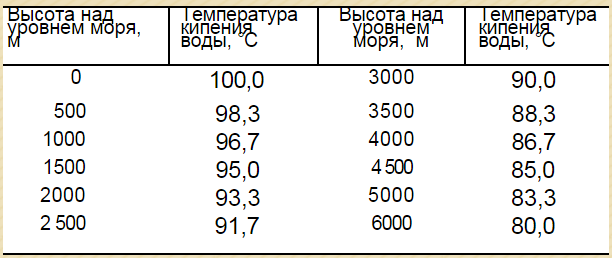
Таблица № 2. «Как будет меняться t° кипения с высотой».
| Высота над уровнем моря | t° кипения |
| 100,0 | |
| 500 | 98,3 |
| 1000 | 96,7 |
| 1500 | 95,0 |
| 2000 | 93, 3 |
| 2500 | 91,7 |
| 3000 | 90,0 |
| 3500 | 88,3 |
| 4000 | 86,7 |
| 4500 | 85,0 |
| 5000 | 83,3 |
| 6000 | 80,0 |
Температура кипения воды в шахте
Если спуститься в шахту, то давление будет увеличиваться.
Температура кипения воды в шахте зависит от глубины (при спуске на 300 м вода закипит при t 101°C, при глубине 600 метров -102 °C
Применение герметической крышки
Герметичные крышки не позволяет образовавшемуся пару ускользнуть. В среднем температура закипания воды увеличивается от 5-20 градусов.
В хозяйстве для приготовления блюд часто используют кастрюли, сковородки с герметичной крышкой. Таким образом, уменьшается время приготовления пищи за счет высокой температуры, а блюда получаются более вкусными. В горных районах с низким давлением это необходимая вещь для приготовления пищи. Так же используют мультиварки и сотейники.
Кипячение воды в вакууме
Вакуум — это среда с газом, с пониженным давлением.
Виды вакуумов:
- низкий;
- средний;
- высокий;
- сверхвысокий;
- экстремальный;
- космическое пространство;
- абсолютный.
Температура кипения воды в вакууме зависит от того, какое давление в нём.
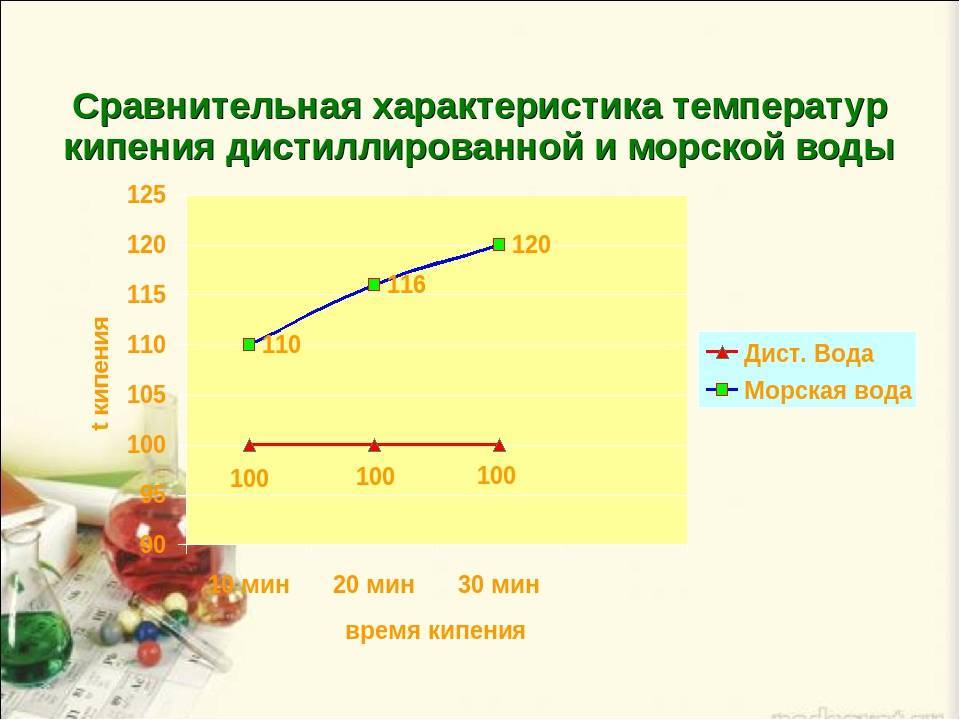
Кипение солёной воды
Солёная вода закипает при более высокой температуре за счет своих свойств.
Соль увеличивает плотность воды, соответственно на процесс требуется больше времени.
t° повышается примерно на 1 градус при добавлении 40 грамм соли на литр воды.
Температура кипения воды в чайнике
Чистая пресная вода закипает в чайнике при t° 100 градусов °C при условиях нормального атм. давления 760 мм ртутного столба.
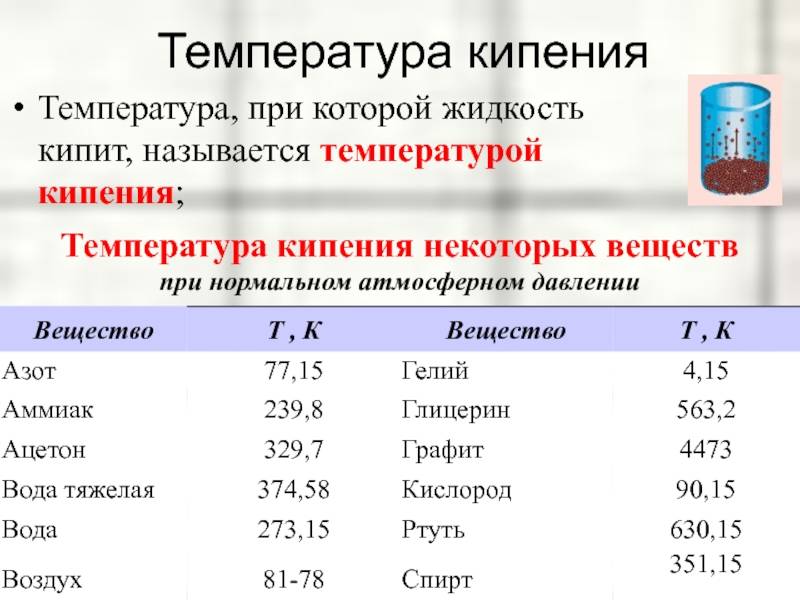
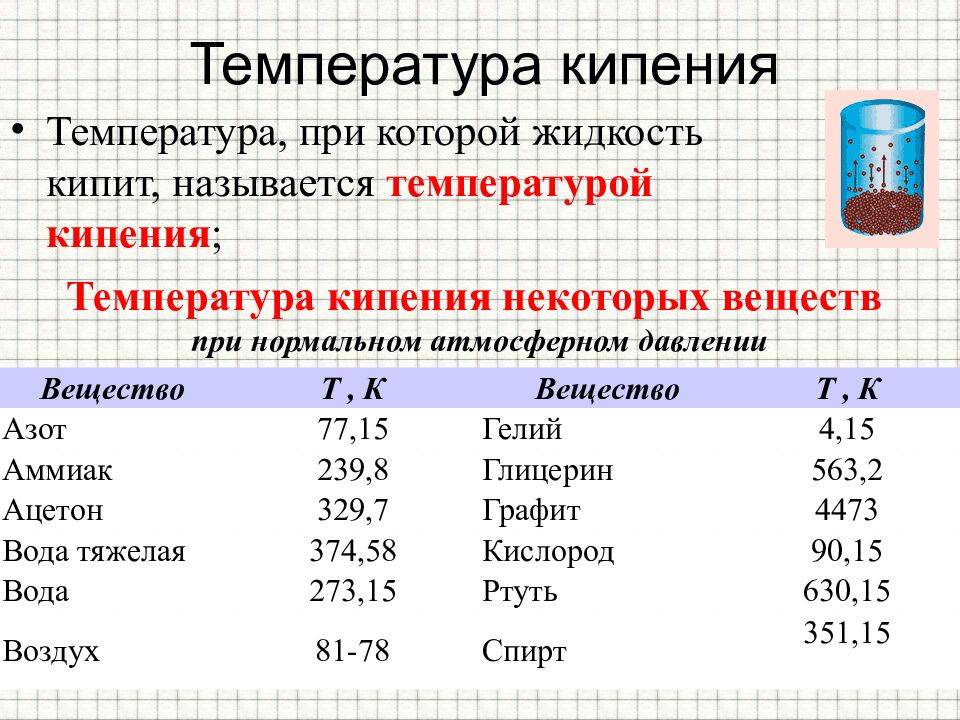
Температура кипения некоторых веществ
В таблице 1 представлены экспериментально полученные значения температуры кипения для различных веществ.
| Вещество | $t_{кип}, \degree C$ | Вещество | $t_{кип}, \degree C$ |
| Водород | -253 | Вода | 100 |
| Кислород | -183 | Ртуть | 357 |
| Эфир | 35 | Свинец | 1740 |
| Спирт | 78 | Медь | 2567 |
| Молоко | 100 | Железо | 2750 |
Талица 1. Температура кипения некоторых веществ (при нормальном атмосферном давлении)
{"questions":[{"content":"Какая температура кипения у свинца?<br />`input-1` $\\degree C$.","widgets":{"input-1":{"type":"input","inline":1,"answer":"1740"}}}]}В обычных условиях кислород является газом. Из таблицы мы видим, что его температура кипения равна $-183 \degree C$. При температуре ниже этой кислород будет жидким.
С другой стороны, вещества, которые мы обычно наблюдаем в твердом состоянии, имеют очень высокую температуру кипения. Например железо плавится и превращается в жидкость при температуре $1539 \degree C$. А чтобы заставить жидкое железо кипеть, необходимо довести его температуры в $2750 \degree C$.
Как кипит H2O в таких условиях?
В любом сосуде, заполненном водой, всегда присутствуют частички воздуха. Они остаются на микроскопических трещинах, имеющихся на стенках емкости. По мере нагрева пузырьки увеличиваются, и становятся видимыми невооруженным взглядом, особенно на стенках сосуда и его дне. По сути, это капли насыщенного пара, растворенные в воде.
На определенном этапе пузырьки под действием силы Архимеда начинают выталкиваться наружу. Вода бурлит, но еще не кипит. Это связано с тем, что нагрев происходит неравномерно.
Когда температура на дне сосуда уже достигла 100 °C, а на поверхности воды ещё нет, сила поверхностного натяжения и атмосферное давление препятствуют выходу частиц за пределы емкости. Они возвращаются назад, теряя температуру.
Когда степень нагрева поверхностного и придонного слоя выравнивается, вещество закипает. В вакууме частицам легче покинуть объем сосуда. Этому препятствует только поверхностное натяжение, поэтому кипение начинается при более низкой температуре.
Процесс кипения
Проведем опыт: будем нагревать воду в открытом стеклянном сосуде и измерять ее температуру.
Отметим, что до того, момента как мы начнем нагревать воду, с поверхности воды идет испарение. Пар при этом не виден глазу, но, тем не менее, существует.
Начнем нагревать воду. Мы заметим, что в воде начинают появляться пузырьки (рисунок 1, а). С повышением температуры они начинают увеличиваться в размерах.
Рисунок 1. Кипение воды
В воде всегда растворено некоторое количество воздуха. При повышении температуры этот воздух выделяется из воды в виде пузырьков. Внутри них — воздух и водяной пар. Водяной пар там присутствует, потому что окружающая вода испаряется внутрь этих пузырьков воздуха.
Когда пузырьки поднимаются в верхние слои жидкости (более холодные), они уменьшаются в размерах. Происходит это из-за конденсации пара внутри пузырьков. Под действием силы тяжести они опускаются вниз в более горячую воду.
И снова начинают подниматься к поверхности. Происходит попеременное увеличение и уменьшение пузырьков, в ходе которых они двигаются в жидкости. При этом мы слышим шум. Он предшествует закипанию воды.
Вода постепенно прогревается по всему объему. Пузырьки перестают уменьшаться в размерах (рисунок 1, б). Под действием архимедовой силы, они всплывают на поверхность и лопаются. Насыщенный пар, содержащийся в них, смешивается с окружающим воздухом. Прекращается шум, остается только бульканье — вода закипела. Температура воды равна $100 \degree C$.
Кинетическая энергия
Кинетическая энергия нагретого водяного пара активно используется в промышленности. В частности, на основе энергии пара работает такое устройство как паровая турбина. Она представляет собой насаженный на вал массивный диск, на котором закреплены лопасти. На эти лопасти поступает пар, нагретый в паровом котле и имеющий температуру около 600 градусов. Этот пар расширяется в сопло, происходит превращение его внутренней энергии в кинетическую энергию направленного движения. Струя пара, обладающая большой кинетической энергией поступает из сопло на лопасти турбины, приводя турбину во вращение.
Водно-спиртовой раствор
Дело в том, что водка не является чистым спиртом, а представляет собой раствор воды, в котором присутствует доля спирта. В зависимости от того, какова эта доля, меняется температура замерзания.
«Разброс» значений, при которых водка подвергается кристаллизации, от -27ºС до -34ºС. Это приблизительные показатели. Чем больше этанола в водке, тем ниже будет предел, когда она сможет превратиться из жидкого алкоголя в, так сказать, «алкогольное мороженое».
Интересно следующее: процесс замерзания идет постепенно, водка загустевает, превращаясь в подобие желе, и только после этого, если температура не меняется, становится твердой. И целиком она почти никогда не замерзает.
Причина: сначала меняют свои характеристики частички воды — они становятся маленькими льдинками. Концентрация спирта в бутылке становится выше, поэтому теперь раствору требуется более низкая температура, чтобы он стал льдом.
Вряд ли в холодильнике возможно создание условий, когда градус понизится до -33 или -40. Это в быту просто технически невозможно, даже если морозильная установка исправна. Поэтому полное превращение в лед вам вряд ли доведется наблюдать, а вот куски льда в бутылке – это вполне вероятно.